研究情報公開(研究1~80)|臨床研究部|国立病院機構熊本医療センター

研究情報公開(オプトアウト)

研究1~80

80. 人工呼吸器管理を行う重症患者の鎮痛に関する看護師の認識
研究の概要
重症患者の鎮痛は、苦痛の緩和やせん妄の予防、鎮静薬の弊害の低減という、QOLの改善には欠かせない面がある。このような背景をもとに、日本版・集中治療室に対する痛み・不穏・せん妄管理のための離床ガイドライン(J-PADガイドライン)では、鎮痛を主体とした鎮痛・鎮静管理を推奨している。一方で、Roseによる先行研究では、疼痛の自己申告ができない患者に対する看護師の疼痛評価ツールの使用頻度が優位に低いことを明らかにしている。つまり、気管挿管された重症患者のように、自己申告が困難な状況での疼痛評価は、十分に行われていない可能性が高いと考えられる。このことに関しては、気管挿管され、疼痛の自己申告ができない患者が多く入院する当院の救命救急センターでも同様の課題が存在する可能性がある。実際に、非言語的に疼痛評価ができるツールの導入を試みたが浸透せず、疼痛評価の方法については、各々の看護師に委ねられている状況である。
このような課題を解決するには、疼痛を自己申告できない患者を受け持つ看護師が、どのような思考過程をもち疼痛の評価を行っているかを明らかにすることが必要と感じた。しかし、医中誌を用い“看護”“鎮痛”“意識”というキーワードで検索を行ったが、気管挿管された重症患者の鎮痛に関する看護師の思いや意識を記載した論文は少なかった。つまり、疼痛の自己申告ができない気管挿管された患者の鎮痛に関する看護師の思考過程は明らかにされていないという事である。そこで、当病棟看護師の鎮痛管理に関する認識を調査し、考察することで、看護師が疼痛の自己申告ができない気管挿管患者に対して、どのような思考過程を持ち看護を行っているのかを明らかにすることができると考えた。また、そのことが、疼痛評価スケールの導入及び定着の一助になると考えた。
対象及び方法
対象:ベナー看護論に基づき、病院救命救急センター看護師の中からクリティカルケア(救命救急センタ一、ICU、CCU)領域経験年数により、「一人前レベル(クリティカルケア領域で2~3年以内の実務経験がある者)」「中堅レベル(クリティカルケア領域で3~5年以内の実務経験がある者)」「達人レベル(クリティカルケア領域で5年以上の実務経験がある者)」に分け、そこからそれぞれ3名ずつ無作為に計9名選出し、研究のためのインタビューに同意を得られた者にインタビューを行う。
研究代表者
救命救急センター看護師 野々原みつ子
当院における研究責任者
救命救急センター看護師 野々原みつ子
問い合わせ先
救命救急センター看護師 野々原みつ子
TEL: 096-353-6501
79. 慢性硬膜下血腫患者のせん妄発症状況と関連因子の実態
研究の概要
慢性硬膜下血腫とは、頭蓋骨の内側で脳を包む硬膜と脳表面間にある静脈が破綻し、ゆっくりと硬膜下に血腫が溜まる状態です。治療は手術療法であり、術後はドレーンが留置されます。手術翌日の頭部CTにて血腫の除去を確認しドレーンは抜去となります。
平成30年度、7階北病棟における慢性硬膜下血腫の穿頭血腫除去術患者は41名でした。ICD-10によるせん妄の診断基準には、意識・注意障害、認知機能の障害、精神運動性障害、睡眠覚醒リズムの障害、感情障害があり、せん妄を発症した高齢患者にみられる臨床症状として、行動に落ち着きがなく、入院治療を受けていることへの理解が困難であり、説明を受けてもすぐに忘れるという症状を認めます。その結果、病棟でも、高齢者が治療上の安静を保てず、点滴やモニタリングなどの身体に装着中の器具を抜去するというような治療継続が困難な状況が生じていました。せん妄ケアには、多くの看護師が困難を感じていましたが、効果的な介入方法を見いだせずにいまし。せん妄は、身体的・心理・環境的要因などの幅広い因子により起こるため、効果的なケアのあり方の探究が続いている現状があります。そこで、7階北病棟における慢性硬膜下血腫のせん妄発症状況と関連する因子の実態を明らかにしたいと考え、本研究を計画しました。
研究の目的と方法
目的:慢性硬膜下血腫のせん妄発症状況と関連する因子の実態を明らかにする
対象:7階北病棟において慢性硬膜下血腫の診断で入院した患者41名
方法:電子カルテを後方的に調査し、過去1年間の慢性硬膜下血腫である患者の入院時から入院3日目において、せん妄 発症者とせん妄未発症者とを分類し、それぞれの環境因子を比較します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いします。本研究にご自身のデータを使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は新たな試料・情報を取得する事はなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載しないため個人が特定されることはありません。
調査期間
調査対象期間:2018年1月1日~2018年12月31日
研究実施期間:倫理委員会承認後から令和3年3月31日
研究成果の発表
調査した患者さんのデータは集団として分析し、学会で発表します、また、個々の患者さんのデータを発表する時も、個人が特定されることはありません。
研究代表者
7階北病棟看護師 宮崎麻美
当院における研究責任者
7階北病棟看護師 宮崎麻美
問い合わせ先
7階北病棟看護師 宮崎麻美
TEL: 096-353-6501
78. 日本版WISC-Vの開発研究
研究の概要と目的
児童用知能検査WISC-Vは、子どもの能力の特徴を理解し、特徴に応じた教育や支援を行うために世界的にもっともよく用いられています。私たちはこの検査の日本版の開発を行っています。
この検査は日常生活や社会生活を健康に過ごされているお子さまの全国的なデ二タをもとにして作成されます。そのためには、年齢、性別、地域の異なるお子さまのデータを幅広く集め、調査する必要があります。
皆さまの調査へのご協力により開発された検査によって、特徴に応じた教育や支援を受けることができ、学校や家庭で主体的に学び、持っている力を発揮できるようになる子どもが、将来大勢いらっしゃると思います。ぜひとも本研究の趣旨をご理解いただき、調査にご協力くださしますようお願い申し上げます。なお、この調査は、埼玉大学におけるヒトを対象とする研究に関する倫理委員会による承認を受けて行われています。
研究の方法
心理アセスメントの専門性を持つ調査実施者が、日本語に翻訳・翻案した米国版WISC-Vを使って、九州・沖縄地域の健康なお子さまに個別に課題を実施します。場所は調査実施者が手配します。
対象とする参加者は12の年齢層(5~16歳)、合計約1200名です。
本研究の参加について
調査への参加は自由意志に基づきます。参加しないことによって不利益を受けることはありません。また、いったん同意された後であっても、いつでも同意を撤回することができ、撤回によって不利益を受けることはありません。
調査する内容
WISC-Vの課題(標準化調査用)
調査期間
研究対象期間:平成30年4月1日~令和元年12月31日まで
研究実施期間:倫用委員会承認後~令和2年3月31日まで
研究成果の発表
研究成果については、参加されたお子さまの氏名などが明らかにならないようにした上で、本検査マニュアル、学会発表や学術雑誌、データベース上などで公に発表します。
研究代表者
埼玉大学教授 名越斉子
当院における研究責任者
心理療法士 演野学
問い合わせ先
- 心理療法士 演野学
TEL: 096-353-6501 - 株式会社日本文化科学社WISC-V係
TEL: 033-946-3391
77. 慢性骨髄性白血病に対する同種移植の後方視的検討
研究の概要
慢性骨髄性白血病(CML)は特効薬であるチロシンキナーゼ阻害剤(TKI)が奏功しますが、急性転化発症例やTKI無効例では同種造血幹細胞移植が唯一の根治的治療です。TKI出現後に当院で施行した慢性骨髄性白血病に対する同種移植の後方視的解析を計画しました。
研究の対象、方法と目的
2006年2月より2018年12月までに当院で行った同種造血幹細胞移植のうち、慢性骨髄性白血病に対して初回同種造血幹細胞移植を行った患者様を対象とします。10症例のカルテデータを元に後方視的に解析することによって、疾患種類、疾患リスク、ドナー、前処置などが予後に与える影響を検討します。TKIの登場後にも症例によっては治癒のために必要とされる同種造血幹細胞移植の経過を詳細に解析することにより、今後の移植治療の成績向上に寄与することが期待されます。
本研究の参加について
本研究により患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認日以後~2021年3月31日(調査対象期間:2006年2月1日~2018年12月31日)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 窪田 晃
当院における研究責任者
血液内科 窪田 晃
問い合わせ先
血液内科 窪田 晃
TEL: 096-353-6501
76. 一般救急-精神科救急連携による地域連携パス構築に関する実務者アンケートの実施
研究の概要
申請者は、厚生労働科学研究(障害者政策総合研究事業)における「精神科救急医療における質向上と医療提供体制の最適化に資する研究(研究代表 杉山直也)」に参加し、分担研究として、「精神科救急と一般救急の医療連携体制強化による医療の質向上と医療提供体制の最適化」に関する調査研究を実施している。その目的は、精神科救急と一般救急の医療連携体制強化であり、その一環として、今年度は「一般救急―精神科救急連携による地域連携パス」の素案構築を目指している。
精神科救急と一般救急の医療連携体制強化を考えるとき、すでに実臨床で行われている連携業務の標準化を図る取り組みは重要であり、身体合併精神科症例(例.精神科病院に入院している患者さんがイレウスや大腿骨頚部骨折に罹患)に関する一方向性連携パスの作成に取り組むことは連携円滑化に資すると考えられる。
従来、精神科領域においても統合失調症や気分障害(うつ病他)など、疾患別に地域連携パスを構築する試みはあった。これらは退院支援の一環として実施されることが多く、患者を中心として、医療や在宅支援サービスなどとの間で実施されることが多い。このほか、認知症については専門施設である精神科と、かかりつけを担う一般科との間で、循環的な連携促進のためパスが導入されることもある。その一方、身体合併症を有する精神科患者の地域連携については、自殺危機介入に関する試案の提示はあるが実務報告はほとんどない。このように、身体合併精神科症例に関する実効的なパス構築はなされていない。
また、全国的に身体合併精神科症例の対応は、一般救急側、精神科救急側の双方で困難を抱えやすいといわれる。ひとつには、一般救急医療と精神科救急医療とのコミュニケーションのむずかしさ、相互の不安があると指摘されており、今回構築を目指す地域連携パスの中では、平成29~30年度厚生労働科学研究障害者政策総合研究事業 分担研究「精神科救急及び急性期医療における一般救急医療との連携の構築に関する研究」成果物であるJapan Emergency Psychiatry Scale- Expert opinion version(JEPS-Ex)を用いることで、精神心理的な側面に関する情報を簡便に伝達出来るように考えており、この点にも今回研究の新規性がある。
これらの背景をもとに、分担班では地域連携パスの構成要素を精査した(別添アンケト参照)。本パスは、身体合併精神科症例の治療において、円滑な地域連携が可能になることを目的としている。このため、入院中に活用される疾患別のクリテイカルパスとは異なり、身体合併精神科症例が施設から施設へと移動する際、標準的に網羅されるべき項目を並べる構造をとる。また、かかりつけ精神科を持つ症例の身体合併症対応を想定するため、救急病院他の治療施設を経てUターンする流れにおける連携円滑化に資する構造を狙う。
これらの構成項目が妥当なものであるか、パスを実際に利用して患者の治療・ケアにあたる実務者からの意見聴取は必須である。このため、今回、実務者に対するアンケート調査の実施を計画する。
研究の目的と方法
研究対象件数:受講者50名以上、見学者20名以上の回答を目標とする。
回答者は、一般救急―精神科救急連携に関する連携課題について実際的な問題意識を有している必要がある。また、全国より広く意見を募る必要もある。このため、一般救急医療部門における精神科疾患の初期評価方法を学ぶ教育コース (Psychiatric Evaluation in Emergency Care、以下PEEC)への受講者ならびに見学者を調査対象とする。PEECコースは、有料で、自己研鎖のために参加する教育コースであり、受講者は連携課題について常に実務上直面することが受講契機となることも多く、一般救急側、精神科救急側の受講者が同時に参加するため、調査場面としては適切と考えられる。
方法としては、コース受講者もしくは見学者に対してアンケート調査用紙を配布し、回答者が記入し提出することでもって調査同意とみなす。択一式の質問項目が20個、自由記載欄が1か所であるため、回答時間は7分程度を設定する。
実施場所及び実施期間
実施場所:宮城県仙台市(日本精神科救急学会公開PEECコース)、岡山県倉敷市(日本総合病院精神医学会公開PEECコース)、熊本県熊本市(第26回・第27回熊本PEECコース)、長崎県佐世保市(第4団長崎PEECコース)、神奈川県横浜市(第19回横浜PEECコース)ほか。
研究対象期間:令和元年10月19日~令和2年3月31日まで
研究実施期間:倫理委員会承認後~令和2年3月31日まで
本審査提出日から、2020年3月末までの期間、全国で実施されるPEECコースのなかで、主催者から調査協力同意を得られたコースとする。
研究代表者
精神科 橋本 聡
当院における研究責任者
精神科 橋本 聡
問い合わせ先
精神科 橋本 聡
TEL: 096-353-6501
75. がん緩和ケアの栄養サポート
研究の概要
近年の我が国において、がんの栄養療法は、がん診療の遂行支援として重要視されつつあります。その中で、がん緩和ケアにおける栄養療法は、病態や症状の緩和のみではなく患者家族の意向を尊重しながら個別性に沿ったサポートを必要とするため、ケア選択やタイミングの判断が難しく、管理栄養士の活動内容やその効果についての報告は多くはありません。
そこで、がん緩和ケア対象患者の状況と管理栄養士の関わりについて実態調査を実施し、が人緩和ケアにおける栄養管理の課題を抽出することで、より質の高い栄養管理につなげることを目的として本研究を計画しました。
研究の目的と方法
本研究は、熊本医療センタのがん緩和ケア対象患者のうち、緩和ケア依頼書の提出があった入院患者さまを対象とし、症例数は45症例を予定しています。がん緩和ケア対象患者さまの状況や栄養管理の実態を調査するため、日常診療で得られた情報(疾患名、症状、治療状況、検査値、食事内容、食事摂取状況、転帰など)を電子カルテより収集し、後向きに解析します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。
本研究にご自身の臨床データを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
実施期間
研究対象期間:平成31年4月1日~令和元年9月30日まで
研究実施期間:倫理委員会承認後~令和2年3月31日まで
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
栄養管理室 北向 由佳
当院における研究責任者
栄養管理室 四元 有吏
問い合わせ先
栄養管理室 北向 由佳
TEL: 096-353-6501
74. Dual Energy CT撮影による胆石の検出能の評価
研究の概要
単純CT撮影においてX線陰性胆石は検出が困難です。しかし、Dual Energy CT撮影し、仮想単色X線画像を取得することにより検出が可能と報告があります。当院で、検出された胆石症例を後向きに描出能を評価し、視認性の優れる描出条件を検討します。
研究の目的と方法
検出された胆石症例を後向きに描出能を評価することを目的とします。
当院でDual Energy CT(管電圧100kV/Snl40kV)撮影した胆石症例を後向きにCT値を測定し、比較します。また視認性の優れる描出条件を検討します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また研究に扱う情報は、個人が特定されない形で、厳重に行います。本研究にご自身のデータの使用をご希望されない方は、あるいはご質問等おありの方は、末尾の問合せ先までご連絡ください。
調査する内容
本研究は、新たな検査をすることはなく、既存カルテ情報のみを用いて実施する研究です。急性胆のう炎などの画像所見を呈する症例のCT検査、MRI検査の内容を調査します。個人情報の取り扱いについては、「人を対象とする医学系研究に関する倫理指針」、「個人情報の保護に関する法律j及ひ適応される法令、条例等を遵守します。研究対象者の情報を取り扱う場合は秘密保護に十分配慮し、特定の個人を識別することができないようにします。
調査期間
研究対象期間:令和1年6月1日~令和1年9月30日まで
研究実施期間:倫理委員会承認後~令和1年12月31日まで
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。個人情報は調査しないので、個人が特定されることはありません。
研究代表者
放射線科 岩元 優樹
当院における研究責任者
放射線科 岩元 優樹
問い合わせ先
放射線科 岩元 優樹
TEL: 096-353-6501
73. オキサリプラチン製剤の後発医薬品メーカー変更に伴うアレルギー発現状況調査
研究の概要
医療費削減や患者負担軽減の観点から後発医薬品の使用が推奨されていますが、後発医薬品の承認申請の際には、製造方法、安定性、薬理試験、生物学的同等性等については審査が行われるものの臨床試験が行われていないため、メーカー間で安全性に違いがでる可能性があります。2018年2月、当院では国立病院機構病院が行っている共同購入に基づきオキサリプラチン(以下、L-OHP)後発医薬品の採用にて製造メーカーがA社からB社へ変更になりました。L-OHPは大腸癌、胃癌、膵臓癌などの化学療法において重要な医薬品ですが、末梢神経障害、アレルギー症状、血管痛などの特徴的な副作用があります。中でもアレルギー症状は気管支痙攣、呼吸困難、血圧低下等の重篤な症状を引き起こすことがあり、治療継続の上で最も問題となる副作用です。L-OHP後発医薬品のメーカー間でのアレルギーの発現状況を調査することで、メーカー間での安全性の違いが確認でき、患者に対してもL-OHPによる安全な治療の提供ができ、治療効果の向上につながると期待できます。かつ共同購入品目選定の上でも安全かつ適切な治療を提供する上でも重要なデータとなり、国立病院機構全体に活かされる事が期待されます。
研究の目的と方法
2017年1月1日から2018年12月31日に当院でL-OHPを開始した愚者を対象とし、患者背景(年齢、性別、疾患名、レジメン名、L-OHPの総投与量等)、アレルギの発現時期、重篤度について電子カルテより調査します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に取り扱します。本研究にご自身の臨床データを研究に使わないで欲しいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先まで、ご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
倫理委員会承認後より2020年3月31日にかけて調査を実施します。〈調査対象期間2017年1月1日から2019年9月 30日)
研究成果の発表
調査した患者さまのデータは、学会や論文で発表しますが、個人が特定されることはありません。
研究代表者
薬剤部 横田千明
当院における研究責任者
薬剤部 横田千明
問い合わせ先
薬剤部 横田千明
TEL: 096-353-6501
72. フェンタニル製剤を使用中に重篤な副作用が生じた2症例
研究の概要
フェンタニル貼付剤や口腔粘膜吸収剤はがん患者の疼痛治療において有用です。しかしながら、呼吸抑制などの重篤な副作用も報告されています。フェンタニルは、動物実験において、他のオピオイドより呼吸抑制が起こしやすいことが示唆されていますが、臨床での報告は少なく、フェンタニル製剤の副作用を集積し、検討する必要があります。今回、当院でフェンタニル製剤を使用中に重篤な副作用が生じた症例について調査を行い、フェンタニル製剤による副作用を防止するための方策について検討することを目的とし、観察研究を計画しました。
研究の目的と方法
本研究では、平成27年6月30日から平成28年1月25日の問に、国立病院機構熊本医療センターでフェンタニル製剤を使用した患者様のうち、重篤な副作用が生じた方を対象としています。日常診療で得られた臨床データ(年齢、性別、使用薬剤、施行した検査、入院経過など)を電子カルテから集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載しませんので、個人情報は特定されません。
調査期間
研究対象期間:平成27年6月30 日~平成28年1月25 日まで
研究実施期間:倫理委員会承認後~令和 1年10月31日まで
研究成果の発表
調査した患者様のデータは、集団として分析し、学会や論文で発表します。また、個々の患者様のデータを発表するときも、個人が特定されることはありません。
研究代表者
薬剤部 尾関あゆみ
当院における研究責任者
薬剤部 尾関あゆみ
問い合わせ先
薬剤部 尾関あゆみ
TEL: 096-353-6501
71. 感染症に起因したDICに対するアンチトロンビン製剤の使用状況調査
研究の概要
アンチトロンビン低下を伴う播種性血管内凝固症候群の(DIC)治療には、血漿由来人アンチトロンビン製剤が使用されています。近年、遺伝子組み換えアンチトロンビン製剤が導入され選択肢が増えています。遺伝子組み換えアンチトロンビンは、血漿由来のウイルス等による感染リスクの低減が期待されている他、血漿由来人アンチトロンビン製剤との比較試験において生物学的同等性およびDIC離脱率に関する非劣性が報告されています。
研究の目的と方法
当院における感染症に起因したDICに対するアンチトロンビン製剤の使用状況を調査し有効性と安全性を評価します。
本研究の参加について
本研究により患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究へ参加されたくない方は、データ登録を拒否して頂くことができます。その場合は、研究責任者へご連絡ください。
調査する内容
本研究は既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
調査対象期間: 2017年6月1日~2019年3月31日
研究実施期間: 倫理委員会承認後~2020年3月31日
研究成果の発表
調査した愚者さまのデータは、集団として分析し、学会や論文で発表を予定しています。
研究代表者
薬剤部 花田聖典
当院における研究責任者
薬剤部 花田聖典
問い合わせ先
薬剤部 花田聖典
TEL: 096-353-6501
70. 熱中症患者の医学情報等に関する疫学調査
研究の概要
暑熱環境による熱中症に関して、夏季になると多数報道されますが、本邦における熱中症、特に重症の場合の実態は、十分に解明されていないのが現状です。本研究は、重症熱中症の全国規模の実態調査であり、原因や病態の解明および治療や予後の実情を把握し、発生の予防に向けた地域医療へのアプローチを検討することを目的に行います。
研究の目的と方法
2019年7月から2019年9月30日までに国立病院機構熊本医療センターにおいて、熱中症と診断された全ての患者さんが対象となります。なお、外来診療のみで帰宅となった患者さんは除外します。診療録の中において、年齢、性別、来院方法、発生状況、現場でのバイタルサイン、既往歴、生活歴、来院時の所見(身体所見・検査所見など)、発生原因、治療法および転帰に関する情報を匿名化して、日本救急医学会熱中症に関する委員会にWeb登録とFAX送信を行います。その後、日本救急医学会熱中症に関する委員会において集計・解析を行い、発生予防を含めた対策について検討を行います。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載しませんので、個人情報は特定されません。
調査期間
研究期間:2019年7月1日~2020年3月31日(調査対象期間:2019年7月~2019年9月)
研究成果の発表
調査した患者さんのデータは、集団として分析し、発生予防を含めた対策について検討を行います。
その成果は学会や論文、熱中症診療ガイドラインの作成などを通して発表されます。
研究代表者
帝京大学医学部附属病院 救急医学講座神田潤
当院における研究責任者
救命救急科 原田正公
問い合わせ先
救命救急科 北田真己
TEL: 096-353-6501
69. ブスルフェクス1回投与法への変更による精神症状への影響
研究の概要
同種造血幹細胞移植の前処置には化学療法、放射線照射が併用されますが、静注ブスルファンはその中心的な薬剤です。従来は1日4回、各2時間の点滴静注が必要でしたが、2018年7月より1日1回の投与が承認され、患者、医療スタッフの負担軽減に寄与しています。1回投与への変更に伴う副作用の発現率等への比較調査を行うものです。
研究の目的と方法
2016年1月から2019年6月までの間に当院で4日間のブスルフェクス投与後に同種造血幹細胞移植を行った患者様に関して、カルテデータを用いて4回投与法と1回投与法による精神症状(幻覚、幻視、幻聴、薬剤介入を要する不安)の発現率、肝障害(血清総ピリルビン、AST、ALT、ALPの上昇)の出現率、全生存率、治療関連死亡率を比較します。
本研究の参加について
本研究により患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認日~2020年4月30日(調査対象期間:2016年1月1日~2019年6月30日)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
薬剤部 眞弓健介
当院における研究責任者
薬剤部 眞弓健介
問い合わせ先
薬剤部 眞弓健介
TEL: 096-353-6501
68. 排尿ケアチームが介入した脳卒中患者の特徴
研究の概要
平成28年診療報酬改定により排尿自立指導料が新設され、当院でも平成30年4月より泌尿器医師、専任看護師、病棟看護師、専任理学療法士、専任作業療法士からメンバー構成された排尿ケアチームラウンドが開始となりました。排尿自立に向けて包括的排尿ケアを実践することで排尿自立ができ、日常生活動作の維持・促進をもたらし、早期退院に繋がります。
研究の目的と方法
平成30年4月から排尿ケアチームが介入した脳卒中患者について、電子カルテから調査、現状分析し特徴を明らかにします。
本研究の参加について
本研究は、カルテデータの分析であるため、患者様へ不利益が生じることはありません。また研究時に扱う情報は、個人が特定されない形で厳重に取り扱いいたします。その他本研究に関してご質問がございます際には、末尾の問い合わせ先までご連絡ください。
調査する内容
患者さんの年齢、性別、尿道留置カテーテル留置期間、下部尿路機能障害の評価項目の排尿自立度点数と下部尿路機能点数、排尿ラウンド回数について調査します。データは過去のカルテから調べるだけですので患者さんの氏名・住所・生年月日など個人を特定する情報は調査しません。
実施期間
研究対象期間:平成30年4月1日~令和3年3月31日まで
研究実施期間:倫理委員会承認後~令和3年5月31日まで
研究成果の発表
第29回日本排尿機能学会で発表する予定です。
研究代表者
看護部 藤川美和
当院における研究責任者
看護部 藤川美和
問い合わせ先
看護部 藤川美和
TEL: 096-353-6501
67. 末梢性T細胞リンパ腫、非特異群及び血管免疫芽球性T細胞リンパ腫に対する移植非適応症例と診断された患者さんの情報を研究に利用することについてのお願い
熊本医療センターでは、下記の臨床研究を実施しております。本研究に関するご質問等がありましたら下記の「問い合わせ先」までお問い合わせ下さい。ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
研究の概要
末梢性T細胞リンパ腫、非特期学及び血管免疫芽球性T細胞リンパ腫に対する移植非適応症例に関する多数例の報告はわが国ではほとんどありません。最近、末梢性T細胞リンパ腫、非特異群及び血管免疫芽球性T細胞リンパ腫に対し新しい薬が開発され、保隣適応となっています。再発・難治の末梢性T細胞リンパ腫、非特異群及び血管免疫芽球性T細胞リンパ腫への使用例が増えることが予想されており、これらの新薬を投与することで再発予防できることが期待され、前向き臨床試験が計画されています。海外でも末梢性T細包リンパ腫、非特異群及び血管免疫芽球性T細胞リンパ腫の症例数は決して多くなく移植非適応症例に限定したものはほとんどありません。データを後方視的解析し、新たな見通しが示されることが期待されます。新薬の影響が少ない時期に発症した症例での新薬治療の適応について参考となるデータを提示します。
研究の目的と方法
研究の目的
末梢性T細胞リンパ腫、非特異群及び血管免疫芽球性T細胞リンパ腫に対する移植非適応症例に関する成人症例の現状を確認することで新規治療開発における基盤となるデータを構築することを目的とします。
研究の方法・対象となる患者さん
2008年1月から2018年4月の期間に末梢性T細胞リンパ腫、非特異群及び血管免疫芽球細胞リンパ腫に対し移植非適応と担当医が判断した16歳以上の患者さん(固形腫瘍や造血器悪性腫瘍後に発症した二次性白血病症例を除く。)について、個人が特定されないように配慮した上でカルテ’情報を収集し解析します。
本研究の参加について
当該研究にカルテ情報が用いられることについて患者さんもしくは患者さんの代理人の方にご了承いただけない場合には研究対象としませんので、下記の[当院の問い合わせ窓口]までお申出ください。その場合でも患者さんに不利益が生じることはありません。
調査する内容
利用するカルテ情報
診断時年齢、性別、診断日、診断病期、PS、病期、最終観察日、転帰、再発の有無、再発日、死亡日、死因、追加治療等
情報の管理
情報は、研究代表者機関である九州医療センターに郵送で提出され、集計、解析が行われます。
実施期間
研究対象期間:2008年1月1日~2018年4月30日まで
研究実施期間:倫理委員会承認後~2023年7月31日まで
研究成果の発表
この研究は、国立病院機構の多施設との共同研究で行われます。研究で得られた情報は、共同研究機関内で利用されることがあります。
研究代表者
国立病院機構九州医療センター血液内科医長 山崎聡
当院における研究責任者
血液内科 河北敏郎
問い合わせ先
血液内科 河北敏郎
TEL: 096-353-6501
66. Daratumumab投与によるInfusion Reaction発現状況に関する調査
研究の概要
再発又は難治性の多発性骨髄腫の治療に用いられるDaratumumabはその重大な副作用一つとして投与時のInfusion Reaction(以下 IR))発現が知られている。IRの予防のため前投薬として副腎皮質ホルモン・抗ヒスタミン薬・解熱鎮痛剤が使用される他、呼吸器・消化器症状の発現抑制を目的としてロイコトリエン阻害剤の併用が行われる。臨床試験においてロイコトリエン阻害剤として主にモンテルカストが使用されていたが、当院ではDaratumumab前投薬にプランルカストを併用しIRの発現予防を実施している。そこで、当院におけるDaratumumab投与時のIR発現状況を把握するために調査を行う。
研究の目的と方法
本研究では、2018年1月から2019年3月までにDaratumumabが導入された患者を対象としています。診療で得られた臨床データ(年齢、性別、Daratumumab投与量、前投薬、IRの有無、IR発現時の対処等)を電子カルテから抽出します。
本研究の参加について
これにより患者様に新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他に研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
実施期間:委員会承認日以後から2020年3月31日まで
研究期間:2018年1月1日から2019年3月31日まで
研究成果の発表
調査した患者様のデータは、集団として分析し、学会や論文で発表します。また、個々の患者様のデータを発表するときも、個人が特定されることはありません。
研究代表者
薬剤部 井上勝光
当院における研究責任者
薬剤部 井上勝光
問い合わせ先
薬剤部 井上勝光
電話 096-353-6501
65. 職員の流行性ウイルス疾患の抗体か管理とワクチン接種に向けた取り組み
研究の概要
流行性ウイルス疾患、(麻疹、風疹、水痘、ムンプス)においては、ワクチン接種により抗体を獲得することで、発症を予防できる疾患です。医療従事者では患者との接触機会が多く、感染を受けた場合に自身への影響はもちろん、媒介し患者へ拡げた場合の影響は大きく、抗体価を適切に管理し、必要な場合ワクチン接種を受けることが望まれます。
研究の目的と方法
2008年12月より2018年12月までに職員健診で、流行性ウイルス疾患の抗体価測定を行った職員を対象として、医療従事者に必要とされる抗体価レベル、およびワクチン接種が必要な職員がどの程度いるのかを後方視的に解析します。
本研究の参加について
本研究により職員に新たな検査費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されないで厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを使用しないでほしいと希望される方、その他研究に関して質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は新たに試料・情報を取得することなく、職員健診の検査結果を用いて実施する研究です。研究対象者(職員)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
実施期間
研究対象期間:平成20年12月~平成30年12月まで
研究実施期間:倫理委員会承認後~令和元年10月30日まで
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
感染制御室 田代里美
当院における研究責任者
感染制御室 田代里美
問い合わせ先
感染制御室 田代里美
電話 096-353-6501
64. 患者情報システムを用いた集中治療部の機能評価
研究の概要
一般社団法人日本集中治療医学会が運営する診療データベース事業(日本ICU患者データベース,Japanese Intensive care Patient Database:JIPAD)です。
研究の目的と方法
JIPAD事業は、集中治療室に入室した患者さんの重症度等の医療情報を収集し、各施設問での比較およひ研究を行うことによって、医療の質の向上および集中治療医学の発展をめざすことを目的としています。
2014年1月以降に当院集中治療室に入室され治療を受けられたすべての方を対象としてJIPADデータベースに情報を登録・提供します。患者さんへの直強的な介入や侵襲はなく、登録によっていかなる利益・不利益も生じません。 情報として、年齢、性別、病名、慢性疾患の有無、入室の形態、手術の有無、重症度を算出するにあたって必要な検査値・測定値、ICU滞在時間、入院期間、人工呼吸器装着時間、処置内容、転帰を収集します。
情報はすべて匿名化され、個人が同定されることはなく適正に管理されます。なお、当事業はその目的からも、海外を含めた他組織の研究者に匿名化された情報を二次利用の形で提供する場合もありますが、その場合も情報は同様に適正に取り扱われます。
また、解析結果は、JIPAD事業が承認した情報のみが集計データの形で公表されます。その集計データから個人が特定されることはありません。
本研究の参加について
当事業への参加は、当院倫理委員会、日本集中治療医学会および外部倫理委員会(ヘルスケア・データサイエンス研究所)の承認を得て行っております。集められた情報については日本集中治療医学会が責任をもって管理します。当院集中治療室は、情報の取り扱いや安全管理に関する法令や取り決め(「個人情報の保護に関する法律」、「人を対象とする医学系研究に関する倫理指針」など)を遵守しております。本事業で集めたデータは我が国においては集中治療医学会に属し、JIPAD事業に参画している施設の医療者、また国外で同様の研究を行いJIPADと共同研究を申し出て学会が認めた者が利用します。
もしもご自身、あるいは家族の情報を当事業に登録されたくない場合には、下記「問い合わせ先」までご連絡下さし。その際は、患者様の情報は削除し、データをJIPAD事業に提供することはありません。また、登録の拒否により何ら不利益を被ることはありません。
JIPAD事業のより詳細な情報は、ホームページ(https://www.jipad.org) に掲載されておりますので、そちらも御覧ください。
実施期間
2014年1月から2023年3月31日まで
研究代表者
京都府立医科大学病院集中治療部 橋本悟
当院における研究責任者
救命救急科 原田正公
問い合わせ先
救命救急科 原田正公
TEL: 096-353-6501
63. 日本航空医療学会ドクターヘリ・レジストリーへの症例登録事業
研究の概要
航空医療学会が行う、ドクターへリで診療された患者様の診療情報登録事業です。
研究の目的と方法
ドクターヘリで診療された患者さまの診療情報を全国の施設から集め、一元的にデータベース化することによって調査を行います。この調査は、我が国におけるドクターヘリによる診療の全体像を把握し、今後の診療における質の向上に役立たせることを目的としております(この調査は、日本航空医療学会が中心となり全国の医療機関と共同で行っています)。
この調査では、担当者が対象となる方のカルテ〈診療記録)等から、搬送日、年齢、症状、重症度、処置、転帰などについて匿名で集計いたします。
本研究の参加について
2015年4月から2018年3月まで、当院へ救急車またはドクターヘリで搬送された患者さま、および2018年4月以降、ドクターへリで搬送された患者様を対象としております。
調査内容をドクターヘリ基地病院である熊本赤十字病院に提供しますが、個人情報は一切含まれておりません。専用の調査票を熊本赤十字病院に提出しますが、当院では調査票は保管せず直ちに破棄します。
また、この調査へご協力いただけない場合にはいつでも拒否が可能です。その場合でも一切診療上の不利益を受けることはございません。下記問い合わせ先までご連絡ください。
実施期間
2015年3月30日~2020年3月31日
研究代表者
東海大学医学部付属病院 猪口貞樹
当院における研究責任者
救命救急科 原田正公
問い合わせ先
救命救急科 原田正公
TEL: 096-353-6501
62. AMR研究センター耐性菌ナショナル・サーベイランス(JARBS)
―「血液由来黄色ブドウ球菌の病原性解析と臨床応用に関する研究(JARBS-SA)」―
―「血液由来黄色ブドウ球菌の病原性解析と臨床応用に関する研究(JARBS-SA)」―
研究の背景および目的
黄色ブドウ球菌は、様々な感染症を引き起こし臨床上重要な細菌ですが、その病原性には多様性があります。 特にメチシリン耐性黄色ブドウ球菌(MRSA)は市中感染型と医療施設関連感染型に大別され、近年では侵襲性感染症から分離される市中感染型MRSA株が増加傾向にあると言われています。しかし、日本においてどのような株が侵襲性感染症を引き起こしているのか、それらがどのような病原因子を保有しているのかはよく分かっていません。そこで、本研究では、血液培養から分離された黄色ブドウ球菌のゲノム解析を行い、同時に臨床情報も収集することでどのような遺伝子学的特徴を持った株が侵襲性感染症を引き起こしているのかを明らかにすること、日本で流行している特有の株(クローン)の特徴を把握することを目的としています。
調査する内容
- 当院において血液培養から分離された黄色ブドウ球菌を、個人が特定できないようにした上で,国立感染症研究所薬剤耐性研究センター(AMRRC)に送付します。病原因子関連遺伝子のPCR調査及びゲノム解析を行います。 コントロールとして、AMRRCが保有するデータベースと照合してゲノムタイプを調査します。
- 研究期間中、黄色ブドウ球菌が分離された入院患者さんの臨床経過を、個人が特定できないようにした上で、AMRRCに送付します。上記①の結果をもとに統計学的解析を行い、黄色ブドウ球菌の遺伝子型や病原因子による感染巣や臨床経過に違いがあるのかを解析します。
使用する情報
菌株が分離された、患者さんの診療録情報(年齢、性別、人種、国籍、海外渡航歴、職業、動物との接触歴、入院日、基礎疾患(糖尿病・透析)、既往歴、人工物(ペースメ-カー・人工関節・人工弁・大動脈弁)の有無、手術歴、デバイス(人工呼吸器・尿道カテーテル・中心静脈カテーテル・末梢静脈カテーテル)の有無、注射剤使用の有無、アトピー性皮膚炎の有無、HIV感染の有無、インフルエンザ罹患歴の有無、感染のタイプ(1.医療関連感染:医療機関・在宅・その他介護施設等、2.市中感染)、感染巣、感染部位、主に使用した抗MRSA薬、退院日、30日死亡の有無など)を使用します。
対象となる患者さんの利益・不利益
この研究は、患者さんの血液培養から検出された黄色ブドウ球菌と、上記のデータを診療録などから調べる研究ですので、対象となる患者さんに利益及び不利益はありません。また、情報は匿名化して収集し、個人情報(国立感染症研究所での通常業務および一般人の知りうる情報と照合して個人を特定できる情報)は調査しないので、個人情報が漏洩する心配はありません。
本研究の参加について
本研究に参加することによって患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。ご自身のデータを本研究に使わないでほしいと希望されるかた、その他研究に関してご質問のあるかたは、末尾の問い合わせ先までご連絡ください。
研究対象期間および研究実施期間
2019年熊本医療センター倫理委員会承認後~2021年3月31日
研究成果の発表
調査した患者さんのデータは集団として分析し、学会や論文で発表する予定です。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
また、本研究で収集,解析するデータは、個人を特定できない匿名化データの共有による国際的な薬剤耐性の研究と対策の推進を各国に呼びかけているOxford Global Burden of Disease Group等への提供と再解析の可能性がありますが、そこでも個人が特定されることはありません。
研究代表者
院長 高橋毅
問い合わせ先
小児科 水上智之
TEL: 096-353-6501
61. New Japan Cardiac Device Therapy Registry
研究の概要
本研究では、心臓植込み型デバイスの植込み時からの情報を1年毎にデータベースに登録します。日本不整脈心電学会で集積されている過去の情報(後向き部分)と本研究で集積した情報(前向き部分)をあわせ、植込み時の臨床背景とその後の予後等を比較することにより、デバイスの植込み適応が適切であったかどうかを判断します。
研究の目的と方法
心臓植込み型デバイスの植込み治療の実態を調査します。それによって、心臓植込みデバイス植込み基準の適性を検討します。
本研究の参加について
本研究により患者様に新たに検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータを用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認日~2023年3月31日(調査対象期間:2006年1月1日~2023年3月31日)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
山口大学医学部付属病院 清水明彦
当院における研究責任者
循環器内科 藤本和輝
問い合わせ先
循環器内科 藤本和輝
TEL: 096-353-6501
60. 当院における悪性リンパ腫に対する同種移植の後方視的解析
研究の概要
化学療法のみでは根治が期待しにくい悪性リンパ腫に対して、ある程度抗がん剤が効いた場合は一般に自家造血幹細胞移植が選択されます。しかし、自家移植では移植前に十分にリンパ腫が抑えられていない限り再発リスクが高いため、化学療法が効かない悪性リンパ腫に対しては根治と長期生存を目指して同種造血幹細胞移植を行います。
研究の目的と方法
2006年1月より2018年12月までに当院で悪性リンパ腫に対して同種移植を行った16歳以上の患者様を対象として、移植後3年での無再発生存率及び全生存率を主要評価項目として解析を行います。病気が治って長期間生存できる可能性に対して、移植前、移植後のどのような因子が影響をあたえるかを、カルテデー夕、移植データをもとに後方視的に解析します。
本研究の参加について
本研究により患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認~2020年3月31日(調査対象期間:2006年1月~2019年3月)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 河北敏郎
当院における研究責任者
血液内科 河北敏郎
問い合わせ先
血液内科 河北敏郎
TEL: 096-353-6501
59. 高血糖緊急症の病態を解明するための後ろ向き観察研究
研究の概要
高血糖緊急症は糖尿病に関連した救急疾患の代表疾患です。当院でも年間20例ほどの患者の診療を行っています。感染症、血管合併症、電解質異常などの病態を合併することが多く、残念ながら予後不良の方も散見されます。非常に重要な病態でありますが、その解析は海外からの報告がほとんどで、本邦での大規模な研究はほとんどみられません。日本人における高血糖緊急の詳細な解析は、今後の高血糖緊急症の診療に多くの情報をもたらし、重要であると思われます。
研究の目的と方法
本研究では、2012年1月1日~2019年3月31日に国立病院機構熊本医療センターで入院治療を受けた患者さんを対象としています。日常診療で得られたデータを電子カルテから集計いたします。
本研究の参加について
本研究により患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に般います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、未尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(年齢、性別、検査値、治療状況、合併症・転帰など)を用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:倫理審査許可日~2022年3月31日(調査対象期間:2014年1月1日~2019年3月31日)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
糖尿病・内分泌内科 西川武志
当院における研究責任者
糖尿病・内分泌内科 西川武志
問い合わせ先
糖尿病・内分泌内科 西川武志
TEL: 096-353-6501
58. アザシチジン皮下注射による注射部位反応に関する調査
研究の概要
アザシチジンは高リスク骨髄異形成症候群の患者において、移植を行わない症例では第一選択薬と位置づけられる薬剤であり、皮下注射や点滴静注で投与されています。皮下注射で投与する際の副作用として注射部位反応が高頻度で発現していますが、好発部位や発現の要因などに関する報告はありません。そこで今回、当院におけるアザシチジンを皮下注射で投与した際の注射部位反応や発現要因について調査・検討します。
研究の目的と方法
本研究では、2016年1月から2018年12月までにアザシチジンを皮下注射で導入された患者を対象としています。診療で得られた臨床データ(年齢、性別、身長、体重、アザシチジン投与量、注射部位、注射部位反応の有無、注射部位反応の種類等)を電子カルテから抽出します。
本研究の参加について
これにより患者様に新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他に研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
実施期間:委員会承認日以後から2020年3月31日まで
研究期間:2016年1月1日から2018年3月31日まで
研究成果の発表
調査した患者様のデータは、集団として分析し、学会や論文で発表します。また、個々の患者様のデータを発表するときも、個人が特定されることはありません。
研究代表者
薬剤部 藤田強記
当院における研究責任者
薬剤部 藤田強記
問い合わせ先
薬剤部 藤田強記
TEL: 096-353-6501
57. 当院で診断した無症候性多発性骨髄腫の後方視的検討
研究の概要
多発性骨髄腫は無症候性(症状がみられない)の聞は治療を行わず経過観察を行いますが、多くの方が経過中に治療が必要となります。無症候性多発性骨髄腫の患者様の経過から、早期に治療が必要な状態になる可能性が高くなる要因を見出し、今後の治療に役立てることを目的としています。
研究の目的と方法
本研究においては2008年1月1日から2018年12月31日の聞に当科で診断された無症候性多発性骨髄腫の患者様を対象としています。電子カルテより日常診療で得られたデータから後方視的に解析します。
本研究の参加について
本研究により患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間(観察期間):診断日~2019年6月30日
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 原田奈穂子
当院における研究責任者
血液内科 原田奈穂子
問い合わせ先
血液内科 原田奈穂子
TEL: 096-353-6501
56. LBC(Liquid-Based Cytology)法を用いた細胞診によるリンパ腫の診断
研究の概要
リンパ節生検の残余組織からLBC法を用いた細胞診標本を作製し、画像検索、免疫細胞化学的検索を加えたリンパ 腫診断の可能性を検討することです。
研究の目的と方法
リンパ腫の診断は通常リンパ節あるいはリンパ節外病変から生検を行い、組織学的診断で確定します。ところが生検が困難な場合や胸水などの体腔液からの標本の場合組織診断ができず、診断・治療が遅れてしまうことになります。ところがこのような場合であっても細胞診標本は作製可能で、しかもLBC法を用いることで検索法の多様性が広がり、確定診断も期待できるようになってきました。今回リンパ節生検組織の残余組織を用いてLBC法による細胞診標木を作製して、画像解析を行うことで客観的情報によるリンパ腫の診断の可能性を検討したいと思います。本研究により組織でも診断困難な低悪性度リンパ腫を少量でかつ低侵襲の穿刺吸引細胞診検体から確定診断する道が開けることになります。
本研究の参加について
ご協力いただきたいのはリンパ節の検査に使用された後の残余検体を上記検査のために使用する同意をいただくことです。通常の診療でおこなわれる検査で得られた検体の残りを利用しますので、更なる負担、危険性はありません。研究への参加は任意ですし、研究への参加に同意しないことをもって不利益な対応はありません。いつでも不利益を受けることなく撤回することができます。
調査する内容
リンパ腫疑いのリンパ節組織から細胞診断標本を作製し、形態学的検索のほか、免疫細胞化学的・分子生物学的検索を行います。今回の遺伝子の検査は、腫瘍細胞に起こった異常を検査するもので、子孫に受け継がれる遺伝子の変化を調べるものではありません。
調査期間
研究期間:倫理審査承認後~2020年3月31日(調査対象期間: 2019年4月~2020年3月)
研究成果の発表
おこなった研究において、研究結果を患者さんご本人にお教えすることは原則的にありません。研究の成果は提供者の氏名等が明らかにならないようにして、学会発表や学術雑誌で公に発表されることがあります。ご不明の点は主治医にお尋ねください。
研究代表者
病理診断科 村山寿彦
当院における研究責任者
病理診断科 村山寿彦
問い合わせ先
病理診断科 村山寿彦
TEL: 096-353-6501
55. 当院における急性前骨髄性白血病の予後
研究の概要
急性前骨髄性白血病(APL)の治療成績はATRAの登場により飛躍的に向上しました。しかし、APL では他の急性骨髄性白血病より出血イベトが多いことが知られており、重大な問題のひとつです。日本成人白血病研究会(JALSG) での臨床治験での出血イベントのデータはありますが、本邦における実臨床での予後や出血イベントのデータは乏しいのが現状です。当院でのAPL症例の予後と出血イベントを検討し、治療成績の改善を検討します。
研究の目的と方法
2006 年から2018年12 月までの聞に、当院で初発のAPLと診断された患者様に対してカルテデータを用いて予後、出血イベントを後方視的に解析 します。
本研究の参加について
本研究により患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認日~2019年10月31日 (調査対象期間:2006年1月~2018年12月)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 平野太一
当院における研究責任者
血液内科 平野太一
問い合わせ先
血液内科 平野太一
TEL: 096-353-6501
54. 当院の緩和ケアチームにおける歯科介入
研究の概要
WHOによる緩和ケアの定義(2002年)では、「緩和ケアとは、生命を脅かす疾患による問題に直面している患者とその家族に対して、痛みやその他の身体的問題、心理社会的問題、スピリチュアルな問題を早期に発見し、適格なアセスメントと対処(治療・処置)を行うことによって苦しみを予防し、和らげることでクオリティ・オブ・ライフを改善するアプローチである。」とされています。最後まで口から食べられるということは、患者さんのQOLを支え、またご家族の安心感、満足感にも繋がります。しかし、緩和ケア患者さんは、全身状態への対応が優先されるため、口腔内に目を向けられる機会は十分とはいえません。こうした状況下において、患者さまの口腔内環境は劣悪化し、口内炎による疼痛、真菌やウイルスによる感染症、口腔感染症などの影響により、義歯の使用が困難になり、摂食不良による低栄養状態、味覚障害、構音障害、審美障害などを引き起こし、患者さまのQOLを大きく損ねています。
本研究では、当院における緩和ケア介入患者さんの口腔内の実態を把握し、「食べる」「話す」等、口腔機能を最後まで維持するためには何をすべきかを検討するため、臨床的観察並びに歯科介入を行っています。
研究の目的と方法
当院における緩和ケア患者さんの口腔内の実態を把握し、より質の高い緩和ケアを提供していくためには何をすべきかを検討することを目的としています。当院では、同意を得た緩和ケア介入患者さまの病室へ往診し評価を行っています。
本研究の参加について
患者さま個人が特定できる内容は一切公表せず、集計した統計データを用いて評価を行います。また、患者さんに侵襲を与える様な医療行為は行わず、患者さまの全身状態を把握しながら負担をかけない範囲で評価を行います。
調査する内容
口腔内に関して気になっていることや歯科介入希望の有無について等の問診、OHATによる口腔内所見、カルチャースワブを用いた口腔カンジダ症検査を行います。また、口腔機能の低下を調べる検査(細菌数の測定、口腔乾燥度検査、舌圧測定等)を行います。
調査期間
研究期間:2017年4月1日~2018年12月31日
実施期間:倫理委員会承認後~2018年12月31日
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さまのデータを発表するときも、個人が特定されることはありません。
研究代表者
歯科口腔外科 中尾美文
当院における研究責任者
歯科口腔外科 中島健
問い合わせ先
歯科口腔外科 中尾美文
TEL: 096-353-6501
53. HLA1座不一致移植に対するATG投与の影響
研究の概要
同種移植ではHLA完全一致のドナーが理想的とされますが、実際に完全一致ドナーが得られない症例も多いのが実情です。HLA不一致移植では移植片対宿主病(GVHD)のリスクが上昇することにより低下することが知られているため、当院ではHLA不一致ドナーからの移植に際してATGを用いてGVHDを予防しています。この研究では、当院におけるHLA不一致移植に対するATG投与の影響を検討します。
研究の目的と方法
2006年1月から2017年12月までの間に、HLA1座不一致のドナーさんから同種骨髄又は末梢血幹細胞移植を行った患者様に関して、カルテデータを用いて無再発・無GVHD生存率、全生存率、治療関連死亡率、再発率、GVHD発症率などを後方視的に解析します。
本研究の参加について
本研究により患者様に新たに検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認日~2019年10月31日(調査対象期間:2006年1月~2018年11月)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 河北敏郎
当院における研究責任者
血液内科 河北敏郎
問い合わせ先
血液内科 河北敏郎
TEL: 096-353-6501
52. 当院における乾燥濃縮人プロトロンビン複合体製剤(ケイセントラ®)の使用状況
研究の概要
ビタミンK拮抗薬使用中の出血傾向を抑制する乾燥濃縮人プロトロンビン複合体製剤(ケイセントラ®)が2017年9月に発売開始となりました。同薬は速やかな抗凝固状態を是正することが可能で、脳出血の患者さまなどに使用することで、致命的な家かを避けることが期待できます。本研究は、当院での同薬の使用状況と、実際の臨床効果を調査することを目的としています。
研究の目的と方法
当院単施設での後方視的検討で、電子カルテから血液検査のデータや、同薬を使用する原因となった疾患名などの情報を抽出します。
本研究の参加について
後ろ向きの観察研究であり、対象患者様のデータを使用させていただきます。また、研究に扱う情報は、個人が特定されない形で厳重に行います。本研究にご自身のデータの使用をご希望されない方は、あるいはご質問等おありの方は、末尾の問合せ先までご連絡ください。
調査する内容
同薬投与による、実際の血液検査データの改善の程度や、血栓性の合併症の発生状況などを調査します。
調査期間
研究対象期間は2018年1月1日から2018年12月12日としています。調査実施期間は倫理委員会承認日から2019年6月末日とします。
研究成果の発表
第41回日本血栓止血学会学術集会で発表いたします。
研究代表者
救命救急科 櫻井聖大
当院における研究責任者
救命救急科 櫻井聖大
問い合わせ先
救命救急科 櫻井聖大
TEL: 096-353-6501
51. ドナー非特異的抗HLA抗体の生着に与える影響
研究の概要
HLA不一致移植ではドナー特異的抗HLA抗体(DSA)により生着が不良であることが知られています。HLA-DP、DQなどのHLAタイピング時に通常測定しない抗原などに対する抗体が生着に負に作用する可能性が考えられますが、実情として十分なデータがありません。当院ではDSAを避けた幹細胞移植を行っていますが、抗HLA抗体の有無による生着への影響を調べます。
研究の目的と方法
2006年から2018年10月までの間に、当院で同種移植(初回)を受けられた患者さまに対してカルテデータを用いて抗HLA抗体の有無、ドナーソース、生着までの日数や合併症などを後方視的に解析します。
本研究の参加について
本研究により患者さまに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号)は記載せず、個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:当院倫理委員会承認日~ 2019年10月31日(調査対象期間:2006年1月~2018年11月)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 平野太一
当院における研究責任者
血液内科 平野太一
問い合わせ先
血液内科 平野太一
電話: 096-353-6501
50. 超急性期脳卒中患者の座位訓練開始基準についての実態調査
研究の概要
脳卒中急性期リハビリテーションは充分なリスク管理のもと発症後早期から積極的な介入が勧められています。脳卒中治療ガイドラインにおいても「不動・廃用症候群予防し、早期の日常生活動作(ADL)向上と社会復帰を図るために十分なリスク管理のもとにできるだけ発症後早期から積極的なリハビリテーションを行うことが強く勧められる。」と述べられており、超急性期から適切な急性期リハビリテーションを行うことが重要です。当院の救命救急センターにおける脳卒中患者は重症例が多く、看護スタッフは脳卒中患者の早期リハビリテーション介入の在り方について悩んでおり、本研究を計画しました。
研究の目的と方法
本研究は当院の救命救急センターの看護師が、脳卒中患者の座位訓練の開始基準をどこに求めているかを明らかにすることで、早期リハビリテーションの在り方について検討することを目的としています。また、2017年10月~2017年11月に国立病院機構熊本医療センターの救命救急センターに脳卒中の診断で入院となった方を対象としています。入院期間に得られた臨床データ(意識レベル、重症度、入院期間など)を電子カルテから集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いします。本研究にご自身のデータを使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は新たな試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
研究対象期間:2017年10月~2017年11月
研究成果の発表
調査した患者さんのデータは集団として分析し、学会で発表します。また、個々の患者さんのデータを発表する時も、個人が特定されることはありません。
研究代表者
救命救急センター看護師 知識美幸
当院における研究責任者
救命救急センター看護師 知識美幸
問い合わせ先
救命救急センター看護師 知識美幸
TEL: 096-353-6501
49. 高齢者急性腹症の臨床的特徴と予後の検討
研究の概要
本邦では平均余命の延長と高齢者人口の増加に伴い、高齢者の急性腹症に対する手術症例が増加しています。高齢者は併存症や主要臓器機能の低下のため、標準治療を受けることが困難な場合も多いのですが、高齢者の急性腹症に対する治療指針が少ないのが現状です。高齢者の急性腹症の臨床的特徴や手術後の転帰を明らかにすることは重要であると考えられます。
研究の目的と方法
本研究では、2008年4月1日~2020年3月31日に国立病院機構熊本医療センター外科で急性腹症に対して手術を受けた患者さまを対象としています。日常診療で得られたデータ(年齢、性別、検査内容、検査値、最終診断、治療状況、転帰など)を電子カルテから集計いたします。
本研究の参加について
これにより、患者さまに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。ご自身のデータを本研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせまでご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は、記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
研究期間:2017年4月1日~2022年3月31日(調査対象期間:2008年4月~2020年3月)
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や学術論文で発表いたします。また、個々の患者さまのデータを発表するときも、個人が特定されることはありません。
研究代表者
外科 美馬浩介
当院における研究責任者
外科 美馬浩介
問い合わせ先
外科 美馬浩介
TEL: 096-353-6501
48. 多施設内視鏡データベース(JED)の構築プロジェクト
研究対象者
2019年4月より2024年12月までに国立病院機構熊本医療センターにおいて内視鏡検査・治療を受けた方
研究協力のお願い
この研究は、日本全国の消化器内視鏡検査・治療情報を登録し、集計・分析することで医療の質の向上に役立て、患者さんに最善の医療を提供することを目指すプロジェクトです。
情報等の使用について、直接に説明して同意はいただかずに、このお知らせをもって研究に関する事項を公開いたします。対象となる方におかれましては、研究の主旨・方法をご理解いただきますようお願い申し上げます。
この研究への参加(試料・情報提供)を希望されない場合、あるいは、研究に関するご質問は下記の問い合わせ先へご連絡ください。
情報の利用目的及び利用方法
この研究は、日本消化器内視鏡学会内に設けられたJapan Endoscopy Database(JED) Project 委員会が主導となり企画された多施設共同研究です。当初は、東京大学医学部附属病院、国立がん研究センター中央病院、北里大学病院、虎の門病院、京都大学医学部附属病院、東京医科歯科大学医学部附属病院、東京慈恵会医科大学葛飾医療センター、埼玉医科大学国際医療センターの8施設(共同研究機関)のみで開始いたしましたが、現在、日本全国の消化器内視鏡検査および治療情報を登録し、集計・分析することで医療の質の向上に役立て、患者さんに最善の医療を提供することを目指すプロジェクトです。この様な内視鏡関連手技の全国規模の情報集積は初めてのこころみであり、患者側だけでなく、医療を提供する側にも大きな利益をもたらすものと考えています。
日本消化器内視鏡学会では、この研究で集められたデータを分析することで以下のことを明らかにすることを目的にしています。
- 内視鏡関連手技を行っている施設診療科の特徴
- 医療水準の評価
- 適正な消化器内視鏡専門医の配置、ならびに消化器内視鏡技師、看護師などのコメディカルの適正な配置
- 早期癌登録に対する精確な情報収集
- 内視鏡検査、治療を受けた方の予後
- 内視鏡検査・治療の医療経済的な情報収集
- これから内視鏡関連手技を受ける方の死亡・合併症の危険性、など
この研究成果は学会発表、学術雑誌およびデーターベースなどで公表します。 研究にあたっては、個人を同定できないように個人情報は削除したり関わりのない記述等に置き換えたりして使用します。
研究の方法について
内視鏡部門システムから別途定める項目を抽出し、匿名化された状態で日本消化器内視鏡学会本部に設置したサーバ内に格納しデータベースを構築し、各種分析を行う。研究期間は、2015年1月1日~2024年12月31日です。
利用し、又は提供する情報の項目
検査日、年齢、性別、ASA Grade、抗血栓薬(使用状況ならびに中止、置換の有無などの詳細)、喫煙歴ならびに喫煙の有無、飲酒歴および飲酒状況、悪性腫瘍、家族歴、多臓器癌既往歴、ヘリコバクター・ピロリ感染状態、内視鏡検査の予定性、外来・入院、検査目的、治療目的、鎮痙剤使用状況、鎮静・鎮痛・麻酔に関する事項、内視鏡の挿入経路、使用スコープ情報、送気の種類、特殊観察法、観察範囲、手技開始・終了時間、手技中、手技後偶発症、30日以内の死亡の有無、実施医師名(医籍番号)、副実施医師名(医籍番号)、内視鏡看護師・技師名、腹部手術歴、生涯大腸内視鏡歴、造影範囲、挿管、胆管・膵管径、挿管難易度、胆管へのアプローチ方法 など
研究対象者又はその代理人の求めに応じて、研究対象者が識別される情報の利用又は他の研究期間への提供を停止すること
研究対象者をなつ方または代理の方で、本研究への情報の利用にご賛同頂けない場合は、情報の利用を停止することができます。停止を求められる場合には下記「研究対象者又はその代理人の求めを受ける方法」にご連絡ください。
研究対象者又はその代理人の求めを受ける方法
当院の研究責任者:
消化器内科 杉和洋
TEL: 096-353-6501
研究主任施設
日本消化器内視鏡学会事務局・Japan endoscopy Database(JED)Project 委員会
TEL: 03-3525-4670
47. 高齢者消化器癌の臨床病理学的特徴と予後の検討
研究の概要
本邦では平均余命の園長と高齢者人口の増加に伴い、高齢者の消化器腫瘍に対する手術症例が増加しています。高齢者は併存症や腫瘍臓器機能の低下のため、標準治療を受けることが困難な場合も多いのですが、高齢者の消化器癌に対する治療指針が少ないのが現状です。高齢者の消化器癌の臨床的特徴や転帰を明らかにすることは重要であると考えられます。
研究の目的と方法
本研究では、2008年4月1日~2020年3月31日に国立病院機構熊本医療センター外科で消化器腫瘍に対して手術を受けた患者さまを対象としています。日常診療で得られたデータ(年齢、性別、検査内容、検査値、最終診断、治療状況、転帰など)を電子カルテから集計いたします。
本研究の参加について
これにより、患者さまに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。ご自身のデータを本研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせまでご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は、記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
研究期間:2017年4月1日~2022年3月31日(調査対象期間:2008年4月~2020年3月)
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や学術論文で発表いたします。また、個々の患者さまのデータを発表するときも、個人が特定されることはありません。
研究代表者
外科 美馬浩介
当院における研究責任者
外科 美馬浩介
問い合わせ先
外科 美馬浩介
TEL: 096-353-6501
46. 透析室における透析開始前のタイムアウトの有効性
研究の概要
透析医療には、透析機器を使用した体外循環を行う治療室としての特殊性があります。そのため、透析に関わる医療者には専門性が求められるとともに、機器や設定の確認不足が重大な事故に繋がる危険性が常に存在しています。そのため、エラーを事前に検出し、事故防止のためのシステムを構築することが透析医療の安全性の向上だけでなく、患者様に対する透析医療・看護の質の向上が期待できます。
タイムアウトとは:透析開始前に、医療者がすべての作業を中止し、透析機器の確認や透析条件など必要事項の確認を行うこと
研究の目的と方法
透析開始前のタイムアウト導入(2017年4月)前後1週間の透析室での発生したインシデントを集計し、件数ならびに内訳の比較し調査します。
本研究の参加について
本研究は、インシデント分析であるため、患者様へ不利益が生じることはありません。また研究時に扱う情報は、個人が特定されない形で厳重に取り扱いいたします。その他本研究に関してご諮問がございます際には、末尾の問い合わせ先までご連絡ください。
調査する内容
透析開始前のタイムアウト導入(2017年4月)前後1年間の透析室での発生したインシデントの件数ならびに内訳を調査します。
透析開始前のタイムアウト導入前(2016年4月から2017年3月)
透析開始前のタイムアウト導入後(2017年4月から2018年3月)
調査期間
研究期間:倫理委員会承認日より2019年3月にかけて調査します。
研究成果の発表
第64回日本透析医学会学術集会・総会で発表する予定です。
研究代表者
看護部 松野順
当院における研究責任者
看護部 深山美香
問い合わせ先
看護部 深山美香
TEL: 096-353-6501
45. がん化学療法に対する制吐剤としてのオランザピンの使用実態調査
研究の概要
本邦において、2017年6月に厚生労働省からオランザピンを抗悪性腫瘍剤(シスプラチンなど)に伴う悪心・嘔吐に対して使用した場合に、保険適応の対象とすることが通知され、使用方法は、原則として他の制吐薬と併用し、1回5mg(最大10mg)を1サイクルにつき6日間までの投与が目安とされた。しかしながら、現時点で国内におけるオランザピンの至適投与量や安全性に関する検討は十分ではないと考えられる。
現状では、実際に処方されている対象や、投与量も10mg~2.5mgと幅広く、投与タイミングなども施設や処方医ごとに異なる。また、投与時期や投与期間に関しても検討の余地があると考えられる。高齢者への非定型抗精神病薬の適応外投与で死亡率が6~7割上昇したとのFDAの報告や日本における認知症患者の大規模観察研究(J-CATIA)[9]において、抗精神病薬投与患者で11週以降の死亡リスクが約2.5倍上昇することが報告されており、高齢者への投与や眠気が生じやすい状況での使用など、安全面で配慮すべき点は少なくない[5- 7.9.10]。日本人における有効克つ安全なオランザピンの使用に関してエビデンスは不足しており、日本がんサポーティブケア学会から、制吐薬としてのオランザピンについての注意喚起[11]が発出されている。オランザピンのCINVに対する使用が保険適応の対象となったことから、実臨床における使用は増加すると考えられ、早期に現状を把握し、実臨床における有効かつ安全な使用につなげることは急務である。また適格基準が厳密に定められたランダム化比較試験では十分に把握できないリアルワールドのデータが得られる意義は大きい。これまで大規模な実態調査の報告はなく、本研究では、使用実態ならびに過度の鎮静や高血糖など薬剤中止に至る有害事象の情報をもとにオランザピンの適正使用に向けた周知を行うため、全国規模の実態調査を実施する。
研究の目的と方法
がん化学療法において制吐薬として使用頻度が増加しつつあるオランザピンの使用状況を全国的に調査することにより、日本人における適正使用の推進に寄与する。計画している具体的な項目は、
①オランザピンの使用実態調査、②高齢者や糖尿病合併患者などハイリスク患者における使用実態と認容性の検討である。
【研究デザイン】後方視的観察研究、アンケート調査
本研究の参加について
調査対象患者
高度あるいは中等度催吐性リスクの抗がん薬治療(注射薬のみを対象とする)が開始され、調査対象期間に実施された化学療法レジメンのコースを完遂した(抗がん薬の中止がない)20歳以上の患者を対象とする
- 調査期間内にオランザピンが使用された最初のコースを調査の対象とする
- オランザピンの使用頻度を把握するため、期間内にHECあるいはMECを受けた患者数(実数)を調査する。
- 治験や医師主導臨床試験参加中の患者は除外とする
調査する内容
【調査項目】
- 患者背景(年齢、性別、癌腫、化学療法歴、制吐療法、併用薬、合併症)
- 制吐薬としてのオランザピンの投与実績(予防投与、追加治療としての投与)
- オランザピンの投与状況(対象レジメン、治療ライン、コース、投与量、投与タイミング、開始時期、投与日数)
- 高齢者(75歳以上)への使用状況
- 眠気が懸念される状況での使用状況
- 糖尿病患者への使用状況
- オランザピンの使用頻度
- 副作用によるオランザピン投与中止や減量の有無と原因
- 制吐効果
- JACCによる注意喚起情報の認知度(調査対象となった患者の診療科の医師、診療科担当の薬剤師および看護師に対する施設内アンケート:担当者による聞き取り)
調査期間
研究期間:倫理委員会承認後~平成31年6月30日まで(調査対象期間:平成30年6月1日から9月30日)
研究成果の発表
本試験の概要、進捗情報、主な結果は福岡大学病院ホームページならびにUMIN-CTRで公開する。また、研究成果の公表にあたっては、研究参加施設の共同発表として報告する。本研究に関する学会報告、論文報告は、研究代表者、研究事務局が協議を行い本研究への貢献度を考慮して決定する。すべての共著者は論文投稿前に論文原稿作成に関し、主たる公表論文は英文誌に投稿する。
研究代表者
福岡大学薬学部臨床薬学教室準教授・福岡大学病院薬剤部 林 稔展
当院における研究責任者
薬剤部 鶴﨑泰史
問い合わせ先
相談窓口(当院)
薬剤部 鶴﨑泰史
〒860-0008 熊本県熊本市中央区二の丸1-5
TEL: 096-353-6501
相談窓口(研究事務局)
福岡大学薬学部臨床薬学教室準教授/福岡大学病院薬剤部 林 稔展
〒814-0180 福岡市城南区七隈8-19-1
TEL: 092-871-6331
44. 薬剤師外来活動状況調査
研究の概要
がん対策基本計画において、化学療法のさらなる充実とチーム医療の推進が謳われ、専門・認定薬剤師等を適正に配置し、患者さんの副作用や苦痛に対して継続的に対応できる診療体制を整備することが目標として掲げられています。国立病院機構熊本医療センターでは平成29年6月より薬剤師外来を設置し、外来化学療法センターで注射用抗がん剤を投与する患者さんに対する継続的な介入および外来で経口抗がん剤を導入する腫瘍内科・外科・消化器内科の患者さんへの初回指導を行っています。そこで今回、これまでの薬剤師外来における薬剤師の活動状況を調査し、その効果や問題点を抽出することで、今後の薬剤師外来の質向上に結びつけることを目的とし、観察研究を計画しました。
研究の目的と方法
本研究では、2017年6月1日から2018年12月31日までの間に、国立病院機構熊本医療センター外来化学療法センターで注射用抗がん剤を投与した患者さんおよび外来で経口抗がん剤を導入した腫瘍内科・外科・消化器内科の患者さんを対象としています。日常診療で得られた臨床データ(年齢、性別、疾患名、抗癌剤投与量、使用した支持療法薬、採決結果など)を電子カルテから集計します。
本研究の参加について
これにより患者さまに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させて頂くことにご理解とご協力をお願いいたします。本研究にご自身のデータを使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
研究期間:倫理委員会承認後~2019年3月31日(調査対象期間:2017年6月1日~2018年12月31日)
研究成果の発表
調査した患者さまのデータは、学会や論文で発表しますが、個人が特定されることはありません。
研究代表者
薬剤部 大橋邦央
当院における研究責任者
薬剤部 大橋邦央
問い合わせ先
薬剤部 大橋邦央
TEL: 096-353-6501
43. 病理診断支援のための人工知能(病理診断支援AI)開発と統合的「AI医療画像知」の創出
研究の概要
平成29年から病理医不足を補う目的で人工知能を使った病理診断システムの開発が始められ、当院も本研究に参加しています。
研究の目的と方法
患者様から採取した組織から作成される病理組織標本を通常は病理医が顕微鏡で観察して診断していますが、そん診断の補助を人工知能(AI)に行わせる病理診断支援AIの開発が本研究の目的です。まず全国から病理標本のデジタル画像・臨床情報を収集し、人工知能に学習させてその診断精度を上げ、実際の診療での使用を目指します。
本研究の参加について
研究に用いる病理標本は数年前の標本で、すでに診断・治療が終了している症例を検討しますので、本研究による患者様の利益・不利益はありません。また個人情報も守られます。もし本研究へ参加されたくない場合は、いつでもデータ登録を拒否していただくことができます。その場合は、下記の当院研究代表者にご連絡ください。登録を拒否したことで、日常の診療などにおいて患者様が不利益を被ることは一切ありません。
調査期間
研究期間:倫理審査委員会承認後~平成31年3月31日(調査対象期間平成7年1月~平成28年12月)
研究代表者
日本病理学会理事長 北川 昌伸
当院における研究責任者
病理診断科 村山寿彦
問い合わせ先
病理診断科 村山寿彦
TEL: 096-353-6501
42. アクリル樹脂を用いた前頭洞閉鎖に関する手術手技の報告
研究の概要
2008年12月から2018年6月までに当院にて全交通動脈瘤に対して開頭クリッピング術を行った患者様の経過を追跡いたします。
研究の目的と方法
私たちは全交通動脈瘤に対して開頭クリッピング術を行った際にアクリル樹脂を用いて前頭洞と呼ばれる副鼻腔を閉鎖し、術後感染を予防しています。術後の合併症の発症率について追跡を行い、手術手技の有用性について提言いたします。
本研究の参加について
これにより患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただく事にご理解とご協力をお願いいたします。本研究でご自身のデータを研究に使わないでほしいと希望される方、その他研究に関してご質問がございます際には、末尾の問い合わせ先までご連絡ください。
調査する内容
全交通動脈瘤に対して開頭クリッピング術を行った患者様の年齢、性別、術後合併症の有無について既存のカルテ情報から調査します。患者様の個人情報につきましては記載いたしません。
調査期間
研究期間及び調査対象期間:2008年12月1日~2018年6月31日
研究成果の発表
調査した患者様のデータは、学会や論文で発表いたします。個人が特定されることはありません。
研究代表者
脳神経外科 松浦 任
当院における研究責任者
脳神経外科 松浦 任
問い合わせ先
脳神経外科 松浦 任
TEL: 096-353-6501
41. リウマチ性多発筋痛症におけるマトリックスメタロプロテアーゼ3の臨床的意義についての検討
研究の概要
リウマチ性多発筋痛症(polymyalgia rheumatica:PMR)は、高齢者に急性発症するリウマチ性疾患で、体幹、四肢近位部のこわばりと自発痛を特徴とする原因不明の炎症性疾患です。一方、マトリックスメタロプロテアーゼ3(matrix metalloproteinase-3;MMP-3)は、様々な、細胞外マトリックスの構成成分を破壊することで、軟骨および骨の破壊に関与する酵素です。MMP-3は、関節リウマチ(rheumatoid arthritis;RA)患者において骨破壊、身体障害の予測因子であることが証明されています。PMRにおいてもRA と同じくMMP-3が上昇することが知られていますが、臨床的意義は明確ではありません。
研究の目的と方法
今回の研究は、PMRにおけるMMP-3の臨床的意義を明らかにすることを目的としています。本研究では、2011年4月1日~2017年12月31日に国立病院機構熊本医療センターを受診された患者さまのうち、①PMR診断基準(Bird ら)を満たし、抗CCP抗体陰性(<0.6)である、②診断時にMMP-3を測定している方を対象としています。日常診療で得られた臨床データ(年齢、性別、検査内容、検査値、最終診断、治療状況、転帰)を電子カルテから集計いたします。
本研究の参加について
これにより患者さまに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。ご自身のデータを本研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は、記載せず、対応表を作成して管理しますので個々じょうほうh
調査期間
研究期間:2018年12月1日~208年12月31日(調査対象期間:2011年4月~2017年12月)
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や学術論文で発表いたします。また、個々の患者さまのデータを発表するときも、個人が特定されることはありません。
研究代表者
総合診療科 辻 隆宏
当院における研究責任者
総合診療科 辻 隆宏
問い合わせ先
総合診療科 辻 隆宏
TEL: 096-353-6501
40. 健常成人におけるサイトメガロウイルス感染症についての検討
研究の概要
サイトメガロウイルス(CMV)感染症は、CMVの初感染、再感染あるいは再活性化によって起こります。健常成人におけるCMV感染症は、伝染性単核症様の症状を呈し、大半は対症療法で軽快しますが、稀に腸炎、溶血性貧血、血小板減少、脳炎といった重篤な病態を呈することがあります。また、我が国の成人におけるCMV抗体保有率が低下しており、健常成人におけるCMV感染症の増加が予想されます。易感染宿主におけるCMV感染症に関しては、多数の報告がありますが、健常成人においては、まとまった報告が少ないのが現状です。
研究の目的と方法
今回の研究は、健常成人におけるCMV感染症の臨床像を明らかにすることを目的とします。
本研究では、2013年1月1日~2017年12月31日に国立病院機構熊本医療センターを受診された患者さまのうち、16歳以上で、伝染性単核症様の症状を有し、CMV-IgM陽性である方を対象としています。日常診療で得られたデータ(年齢、性別、検査内容、検査値、最終診断、治療状況、転帰)を電子カルテから集計いたします。
本研究の参加について
これにより、患者さまに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。ご自身のデータを本研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせまでご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は、記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
研究期間:2018年12月1日=2018年3月31日(調査対象期間:2013年1月1日~2017年12月31日)
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や学術論文で発表いたします。また、個々の患者さまのデータを発表するときも、個人が特定されることはありません。
研究代表者
総合診療科 辻 隆宏
当院における研究責任者
総合診療科 辻 隆宏
問い合わせ先
総合診療科 辻 隆宏
TEL: 096-353-6501
39. 頻脈性心房細動へのランジオロール投与に対してのクリティカルパス作成の意義と有用性の検討
研究の概要
術後患者の頻脈性不整脈時のみならず、多くの診療科の一般病床でも頻脈性心房粗細動合併時にランジオロールを使用する機会が増えてきたが、本来の適応からはずれた使用や心拍数安定後も長期間に渡り継続使用するなどの問題点も出てきています。ランジオロールの長期間の使用のため、診断群分類による包括支払い制度上も出来高算定よりかなりマイナスとなる例が散見されました。そのためランジオロールの投与方法と観察項目、内服への適切なタイミングでの切り替えを示すパスを作成し、院内で投与方法の標準化をはかることは意義のあることと考えます。
研究の目的と方法
ランジオロールの投与方法と観察項目、内服への適切なタイミングでの切り替えを示すパスを作成し、院内で投与方法の標準化をはかることが、入院期間や医療費などに与える影響があるかを検討することを目的とします。
頻脈性心房粗細動に対してランジオロールの投与をおこなった患者の診療記録より登録患者の臨床背景因子の調査をおこない、包括支払いと出来高算定での医療費や入院期間、ランジオロールの使用期間、本数などを診療科やパス作成前後などで分け、比較検討していきます。
本研究の参加について
頻脈性心房粗細動に対してランジオロールの投与が確認できた入院患者で本登録観察研究に不同意の意思を表明された患者を除く症例を登録します。本事業への参加は、患者さまの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否していただくことができます。その場合は、病院の担当医または下記問合せ先にご連絡ください。なお、登録を拒否されたことで、日常の診療などにおいて患者さまが不利益を被ることは一切ございません。
調査する内容
臨床背景因子(性別、年齢、合併症、身体所見、血液検査データ、投薬内容等)の調査をおこない、包括支払いと出来高算定での医療費や入院期間、ランジオロールの使用期間、本数などを診療記録より調べます。患者さまの氏名・住所・生年月日など個人を特定する情報は解析用データファイルには記載せず、連結可能匿名化し管理します。データは過去のカルテから調べるだけですので、新たな情報の聴取や採取はありません。
調査期間
研究期間:2016年11月1日~2017年10月31日(調査対象期間:左記と同様)
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や論文では発表します。個人情報は調査しないので、個人が特定されることはありません。
当院における研究責任者
循環器内科 宮尾 雄治
問い合わせ先
循環器内科 宮尾 雄治
TEL: 096-353-6501
38. 当院におけるカテーテル関連血流感染症(CRBSI) -現状と意識付け-
研究の概要
当院では、感染症対策チーム(ICT;Infection control team)が厚生労働省院内感染対策サーベイランス(JANIS)の判定基準に基づき、中心静脈カテーテル留置症例において血液培養陽性であった場合に各症例に対してフィードバックを行っていますが、臨床的敗血症(CSEP;Clinical sepsis)の発生状況や治療については明確ではありません。そこで当院における中心静脈カテーテル留置症例の現状を調査し、より適切な管理ができるよう検討しました。
研究の目的
本研究の目的は、当院で中心静脈カテーテルを留置した患者様の実態を調査し、今後の治療の改善を検討するために行われます。
本研究の参加について
本研究へ参加されたくない場合は、データ登録を拒否して頂くことができます。その場合は、研究責任者へご連絡ください。なお、登録を拒否されたことで、日常診療等で患者さまが不利益を被ることは一切ございません。
調査する内容
年齢、性別、カテーテル留置部位、留置期間、カテーテルの種類、留置後38℃以上の発熱の有無と発熱までの日数、血液培養の有無、血液培養検出菌種、CRBSIの診断の有無、転帰について調査を行います。氏名・住所・生年月日などの個人情報は含みません。
対象となる患者さまの利益・不利益
本研究は、患者さまのデータを電子カルテ内のデータベースから情報を抽出し、調査するのみですので、対象となる患者さまに利益及び不利益はありません。データ抽出後、解析を行う際に患者IDなどの個人情報は削除しますが、ファイル等はデータの漏洩がないよう十分注意して取り扱います。
調査期間
2017年1月1日から2017年12月31日に当院で中心静脈カテーテルを留置した患者さまの調査を行います。
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や論文で発表します。患者IDなどの個人情報は削除された状態で分析しますので、個人が特定されることはありません。
研究代表者
救命救急科 山田成美
当院における研究責任者
救命救急科 山田成美
問い合わせ先
救命救急科 山田成美
TEL: 096-353-6501
37. CHDF療法中のDIC患者に対するリコンビナントトロンボモジュリン投与時の出血関連の有害事象発現状況調査
研究の概要
播種性血管内凝固症候群(DIC)の治療薬であるリコンビナントトロンボモジュリンは、以前まで透析患者さまに対しては減量投与が推奨されていましたが、再審査の結果により添付文書が改訂され通常量での投与が可能となりました。しかしリコンビナントトロンボモジュリン投与中に注意が必要な副作用の一つに出血があります。添付文書には「患者の状態に応じて適宜減量して投与する」旨の記載がありますが、持続的血液濾過透析(CHDF)導入時の出血リスクを考慮した明確な減量基準の記載はありません。
研究の目的と方法
持続的血液濾過透析療法中にリコンビナントトロンボモジュリンを投与した患者さまについて、出血関連の副作用の発生状況を調査します。
本研究の参加について
本研究により患者さまに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究へ参加されたくない方は、データ登録を拒否して頂くことができます。その場合は、研究責任者へご連絡ください。
調査する内容
本研究は既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さま)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
調査対象期間:2015年8月~2018年7月
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や論文で発表を予定しています。
研究代表者
薬剤部 花田聖典
当院における研究責任者
薬剤部 花田聖典
問い合わせ先
薬剤部 花田聖典
TEL: 096-353-6501
36. 精神科に入院となった急性薬物中毒患者における、入院後身体合併症の頻度の検討
研究の概要
急性薬物中毒の方が入院となる場合、身体科と精神科のどちらが主治科になるべきか、明確な決まりはありません。精神科で入院となった場合に心配なことは、入院後に重度の身体合併症が生じることだと思います。
研究の目的と方法
当院では急性薬物中毒の方が入院される際には、精神科か救命救急・集中治療部が主治科になりますが、院内ルールに則って主治科を決めています。精神科で入院となった場合に、入院後に重度の身体合併症が起きていないかを調べることで、現在の院内ルールが妥当であるかを調査することを目的としています。
本研究の参加について
後ろ向きの観察研究であり、対象患者様のデータを使用させていただきます。
調査する内容
精神科で入院となった急性薬物中毒の方のうち、入院後に重度の身体合併症を発症した方について、合併症の病名や発症頻度、重症度などを調査します。
調査期間
2017年1月1日~2017年12月31日の1年間
研究成果の発表
第26回 精神科救急医学会で発表いたします。
研究代表者
救命救急科 櫻井聖大
当院における研究責任者
救命救急科 櫻井聖大
問い合わせ先
救命救急科 櫻井聖大
TEL: 096-353-6501
35. 高齢者に対するFlu/BU4/CA/TBI4による骨髄破壊的前処置を用いた臍帯血移植
研究の概要
同種移植の対象年齢は年々高まっていますが、高齢者に対する適切な前処置法は確立していません。当院では56歳以上の血液腫瘍に対する臍帯血移植に際してフルダラビン(Flu)/ブスルファン(BU4)/シタラビン(CA)/全身放射線照射(TBI4)による骨髄破壊的前処置を用いており、その有用性を検証します。
研究の目的と方法
2013年6月から2017年12月までの間に当院でFlu/BU4/CA/TBI4の前処置を用いて初回臍帯血移植を施行した患者様に関して、カルテデータを用いて後方視的に解析します。
本研究の参加について
本研究により患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問合せ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:2018年9月22日~2019年3月31日(調査対象期間:2013年6月~2019年3月)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 河北敏郎
当院における研究責任者
血液内科 河北敏郎
問い合わせ先
血液内科 河北敏郎
TEL: 096-353-6501
34. 同種移植後サイトメガロウイルス感染のリスク因子
研究の概要
同種移植後のサイトメガロウイルス(CMV)感染に対して定期モニタリングによる先制治療が標準的に用いられてきましたが、長期の抗CMV薬投与による副作用や薬剤介入前のCMV感染症が問題となってきた。これまでにも国内外でCMV感染に関するリスク因子の解析は行われてきましたが、本邦で多い臍帯血移植やATLに対する移植で十分な評価が行われているとは言えません。
研究の目的と方法
2014年1月から2017年12月までの間に当院で同種移植を行い30日以上生存し、ドナー及びレシピエントのCMV抗体が判明し、CMV予防を行っていない患者様に関して、カルテデータを用いて後方視的に解析します。
本研究の参加について
本研究により患者様に新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問合せ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者様)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
研究期間:2018年9月22日~2019年3月31日(調査対象期間:2014年1月~2019年3月)
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
血液内科 河北敏郎
当院における研究責任者
血液内科 河北敏郎
問い合わせ先
血液内科 河北敏郎
TEL: 096-353-6501
33. CHASER療法におけるアピレピタント使用状況調査
研究の概要
CHASER療法は再発・難治性B細胞リンパ腫に対する末梢血への幹細胞動員を兼ねたサルベージ療法であり、国内第2相試験において高い奏効率と良好な忍容性を示しています。制吐薬適正使用ガイドラインにおいて、高度催吐性リスクの注射抗がん薬に対してはアプレピタントを含む制吐療法の使用が推奨されていますが、CHASER療法では高用量のデキサメタゾンを使用するため比較的消化器毒性の出現率は低く、アプレピタントによる効果ははっきりわかってません。そこで今回、当院にてCHASER療法を施行された患者におけるアプレピタント使用状況を調査し、その効果や問題点を抽出することで、今後のCHASER療法の質向上に結びつけることを目的とし、観察研究を計画しました。
研究の目的と方法
本研究では、2014年4月1日から2018年3月31日までの4年間に、国立病院機構熊本医療センターにてCHASER療法を施行された方を対象としています。日常診療で得られた臨床データ(年齢、性別、疾患名、抗癌剤投与量、使用した制吐薬、採決結果など)を電子カルテから集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させて頂くことにご理解とご協力をお願いいたします。本研究にご自身のデータを使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
研究期間:2018年12月1日~2019年3月31日(調査対象期間:2014年4月~2018年3月)
研究成果の発表
調査した患者さんのデータは、学会や論文で発表しますが、個人が特定されることはありません。
研究代表者
薬剤部 大橋邦央
当院における研究責任者
薬剤部 大橋邦央
問い合わせ先
薬剤部 大橋邦央
TEL: 096-353-6501
32. C型肝炎治療における医薬連携モニタリングシートの活用とその効果
研究の概要
現在、C型肝炎の治療はインターフェロンフリー治療(direct anti-viral agents;DAAs)治療が主流になっています。当院では原則9日間の入院でDAAs治療を開始し、その後、外来・通院での治療を行っています。DAAs治療はきちんと決められたとおりに服用を継続することが重要であり、治療を安全に完遂するには、副作用の把握、併用禁忌・注意薬の確認、服薬管理が必要で、全治療期間で薬剤師が積極的に関与することが求められています。そこで医療機関および調剤薬局で円滑に情報を共有し、安全なDAAs治療を提供することを目的として、2017年5月より当院の近隣2調剤薬局とモニタリングシートの運用を開始しました。モニタリングシートの運用開始後の副作用の発現状況、併用薬の情報の調査を行い、モニタリングシートの改訂を行っていくことで、患者様に対するケアの質の向上、医療安全への貢献が期待できます。
研究の目的と方法
2017年5月から2018年10月までにC型肝炎でDAAsの治療を行った患者様を対象としています。当院および調剤薬局の薬剤師が患者様との面談の中で聴取した併用禁忌・注意薬の中誌状況、副作用と思われる症状の発現時期・発現率、治療期間中の薬剤の追加状況について調査します。モニタリングシートの記載内容と電子カルテからデータを集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に取り扱います。本研究にご自身の臨床データを研究に使わないで欲しいと希望されている方、その他研究に関してご質問がございます際には、末尾の問い合わせ先までご連絡ください。
調査期間
倫理委員会承認日より2019年3月にかけて調査します。
研究成果の発表
第28回日本医療薬学会年会で発表する予定です。
研究代表者
薬剤部 横田千明
当院における研究責任者
薬剤部 横田千明
問い合わせ先
薬剤部 横田千明
TEL: 096-353-6501
31. 急性期脳梗塞における緊急血行再建術の成績及び予後に関する研究
研究の概要
血栓という血の塊や動脈硬化のプラーク等によって脳の大きな血管が閉塞し広い範囲に脳梗塞が完成してしまった患者様の予後は非常に悪く、死亡や存命してもその後遺症により日常生活動作の低下に伴い、寝たきり生活を余儀なくされていることが多いと言われております。そのため、急性期の脳梗塞患者様においては、日本でも2005年からアルテプラーゼ(グルトパ®、アクチバシン®)という詰まった血管を溶かす点滴のお薬が適応となり、発症4.5時間以内で適応を満たせば使用可能になり有効性を認めております。しかし、アルテプラーゼ投与のみでは効果が充分とは言いきれない患者さんも数多く存在することが事実です。そのため、近年では閉塞した血管に直接、血管の中にカテーテルという管を入れて閉塞した血管を開く脳血管内治療も適応を加味して行われてきており,2015年に世界的な研究でその有効性と安全性が確立され現在も様々な研究がおこなわれております。
熊本県内でも複数の施設で脳血管内治療が可能となってきておりますが、全国的にも地域格差のある治療であり、熊本県としての患者数や治療成績などが明らかになっていないのが現状です。
研究の目的と方法
本研究における目的は、熊本県内の緊急血行再建術における患者様の数や治療成績および予後を明らかにすることです。
熊本大学医学部附属病院脳神経内科、済生会熊本病院神経内科、熊本赤十字病院神経内科、国立病院機構熊本医療センター神経内科に入院した患者様において、緊急血行再建術を行った患者様について術前後の経過をカルテで確認します。検査や治療の方針については、本研究の参加の有無には一切左右されることはありません。あくまで担当医師が判断して、その時点での最善を尽くします。入院中の状態に加えて、治療から3ヵ月後にはどのようなご生活をされているか転帰調査をおこないます。転帰調査は、外来カルテやかかりつけの先生への問い合わせによっておこないますが、詳細がわからない際に、お電話等により直接ご連絡差し上げることがあります。
本研究の参加について
この研究は、患者様の臨床情報を収集して解析する「観察研究」ですので、研究そのものによって生ずるリスクは一切ありません。
患者様がこの研究に参加されるかどうかは、患者様ご自身の自由な意思で決定されます。たとえ参加に同意されない場合でも患者様は一切不利益を受けず、これからの治療に影響することはありません。また、いつでも研究への参加を取り消すことができます。もしこの研究に情報を提供することをお断りになる場合には、下記の問い合わせ先までお電話ください。
調査する内容
患者さんの年齢や性別、既往歴や内服薬、画像検査,血液検査などの検査データ、治療までの時間と内容、治療成績と治療後の経過などの情報を調査します。これらの情報は患者様が特定できない様に匿名化して取り扱います。患者様の氏名・住所・生年月日など、個人を特定しやすい情報は調査しません。
調査期間
研究期間:倫理委員会承認後~2023年3月31日(調査対象期間:2013年1月1日~2023年3月31日)
研究成果の発表
調査した患者さんのデータは集団として分析され、学会や論文で発表される機会があります。しかし、個人が特定されることはありません。
研究代表者
熊本大学脳神経内科 中島誠
当院における研究責任者
脳神経内科 幸崎弥之助
問い合わせ先
脳神経内科 幸崎弥之助
TEL: 096-353-6501
30. 多発性骨髄腫に関する多施設共同後方視的調査研究
研究の概要
日本骨髄腫研究会は1990年1月から2000年12月までの間に受診した症例を調査し、合計1380例についての臨床所見ならびに治療成績を報告した。さらに、日本骨髄腫学会は2001年1月から2012年までの2234例を調査し、新規薬剤の使用により治療成績が著しく向上したことを報告した。その後、わが国においても新規薬剤の承認により、治療戦略は大きな変貌を遂げていることから、日常診療における多発性骨髄腫の治療成績を継続的に調査することは意義が大きいと考えられる。
そこで、我が国における治療の現状とその成績を後方視的に解析し、各種治療法の有効性を明らかにするとともに、今後の治療戦略の確率に寄与することを目的として本研究を計画した。
研究の目的と方法
本疫学観察研究では、以下の点について明らかにすることを目的とする。
- 我が国における多発性骨髄腫患者に対する治療内容とその成績
- 欧米の治療成績との比較による各治療法の有効性と安全性
- 新規治療薬の時代における予後因子
調査方法
参加施設は事務局ホームページから調査ファイル(Excel形式)をダウンロードし、データを入力した上で事務局まで送付する。事務局は調査ファイルを収集し、データを解析する。
本研究の参加について
- 調査対象:多発性骨髄腫(原発性形質細胞白血病を含む)の症例(初診時に無症候性であっても調査期間中に進展し治療を行った例は対象とする)
- 対象:2013年1月1日から2016年12月31日の間に受診した新規例
2001年1月1日から2012年12月31日の間に受診し、前回調査の登録数
本臨床研究は、「人を対象とする医学系研究に関する倫理指針」(平成26年度文部科学省・厚生労働省告示)における「人体から取得された試料を用いない研究」(第5章-第12-1-(2)-イ)に分類される。診療録などの既存資料のみを用いた観察研究であるため当該指針に則り患者からの同意取得は必須とされていないため個別のインフォームド・コンセントは取得しない。本研究の周知(情報の公開)に関しては、日本骨髄腫学会ホームページを用いて、本家球における資料の収集・利用の目的及び内容、研究の方法等を公開するとともに、事務局において本研究の問合せや質問等に対応できる体制を設ける。
調査する内容
調査項目:診断時の以下の臨床所見を調査する。
生年月日、年齢、性、Performance status、臨床症状、M蛋白型、Durie & Salmon病期、国際病期分類(ISS)、腫瘤形成の有無、骨病変の程度、血算、末梢血形質細胞割合、骨髄形質細胞割合、血清アルブミン、クレアチニン、β2-microglobulin、LDH、CRP、免疫グロブリン定量値、血清遊離軽鎖(定量、κ/λ比)、染色体・遺伝子異常、治療レジメン、有害事象とグレード、効果判定(sCR、CR、VGPR、PR、SD、PD)、維持療法、サルベージ治療レジメン、診断日、治療開始日、再発日、最終生存確認日、死亡日
調査期間
研究期間:2017年7月27日~2018年12月31日(調査対象期間:2001年1月~2017年12月)
研究成果の発表
日本骨髄腫学会の業績として、国内外の学会および学会誌に発表する。
研究責任者
群馬大学大学院保険学研究科生体情報検査科学講座 村上博和
〒371-8514 群馬県前橋市昭和町3丁目29-22
TEL: 027-220-7111
Email: hmura@gunma-u.ac.jp
研究代表者(研究統括)
掛川市・袋井市病院企業団立中東遠総合医療センター 名倉英一
〒436-8555 静岡県掛川市菖蒲ヶ池1番地の1
TEL: 0537-21-5555
FAX: 0537-28-8971
Email: nagura-e@chutoen-hp.shizuoka.jp
当院における研究責任者
血液内科 日髙道弘
問い合わせ先
血液内科 日髙道弘
TEL: 096-353-6501
29. 横紋筋融解症による急性腎障害の発症の危険因子に関する検討
研究の概要
横紋筋融解症は、薬剤や外傷による筋肉の挫滅などで起こり、急性腎障害を引き起こす疾患のひとつです。横紋筋融解時の急性腎障害の発症の危険因子は脱水、敗血症、アシドーシスなどと言われています。また血液検査のCK(クレアチンキナーゼ)値が20000IU/L以下では急性腎障害の発症の危険性は低いといわれています。
研究の目的と方法
本研究の目的は、当院でこれまで横紋筋融解を発症(CK値10000IU/L以下)した患者様の実態を調査し、今後の治療の改善を検討するために行われます。
本研究の参加について
本研究へ参加されたくない場合は、データ登録を拒否して頂くことができます。その場合は、研究責任者へご連絡ください。なお、登録を拒否されたことで、日常診療等で患者さまが不利益を被ることは一切ございません。
調査する内容
年齢、性別、横紋筋融解を引き起こした原因、最大CK値、慢性腎臓病の有無、高カリウム血症の有無、最低pH、敗血症の有無、昇圧剤使用の有無、炭酸水素ナトリウム使用の有無、転帰(急性腎障害発症の有無、透析治療の有無、退院時死亡の有無)について調査を行います。氏名・住所・生年月日などの個人情報は含みません。
対象となる患者さんの利益・不利益
本研究は、患者さまのデータを電子カルテ内のデータベースから情報を抽出し、調査するのみですので、対象となる患者さまに利益及び不利益はありません。データ抽出後、解析を行う際に患者IDなどの個人情報は削除しますが、ファイル等はデータの漏洩がないよう十分注意して取り扱います。
調査期間
2017年1月1日から2018年12月31日に当院で横紋筋融解を発症した患者さまの調査を行います。
研究成果の発表
調査した患者さまのデータは、集団として分析し、学会や論文で発表します。患者IDなどの個人情報は削除された状態で分析しますので、個人が特定されることはありません。
研究代表者
救命救急科 原田正公
当院における研究責任者
救命救急科 原田正公
問い合わせ先
救命救急科 原田正公
TEL: 096-353-6501
28. 糖尿病血管合併症と耳朶皺襞の関連に関する後向き解析
研究の概要
糖尿病合併症の予防は糖尿病治療において最も重要な目的の一つです。糖尿病合併症の予防のためには、適切な血糖管理や脂質異常症をはじめとした他の危険因子の管理とともに、糖尿病合併症の発症の有無や進行度を正確に評価する必要があります。
糖尿病血管合併症は大きく二つに分けられます。一つは細小血管合併症と呼ばれており、この中には網膜症、腎症、神経障害があります。糖尿病の発症がない限り発症しない合併症で、糖尿病に特有の合併症と呼ばれています。もう一つは大血管合併症(動脈硬化症)です。狭心症、脳血管障害、末梢動脈疾患などが含まれ、糖尿病でない方にも認められますが、糖尿病の患者さんでは糖尿病でない方に比べ、その発症率が数倍高いといわれています。
ところで、患者さんを診察した時に、耳朶(たぶ)を後下方に走る深い皺(しわ)を認めることがあります。この身体所見を私たちは耳朶皺襞(じだすうへき)と呼んでおり、以前より、冠動脈疾患(狭心症や心筋梗塞)の発症と関連することが報告されていました。
しかし、糖尿病患者でも耳朶皺襞が冠動脈疾患と関連するのか、冠動脈疾患以外の動脈硬化性疾患(脳血管障害や下肢動脈疾患)と関連するのかについてはあまり知られていません。また細小血管合併症については耳朶皺襞と網膜症の関連は認められなかったとの海外の報告がいくつかありますが、日本人での報告や網膜症以外の細小血管合併症との関連についての報告はないようです。
研究の目的と方法
今回の研究では、当院、糖尿病・内分泌内科に入院歴のある2型糖尿病の患者さんのカルテのデータを解析し、耳朶皺襞の有無と動脈硬化症および細小血管合併症の関連について後向き解析を行います。
本研究の参加について
本研究により患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存のカルテデータ(問診記録、身体所見、検査データ)を用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号)は記載せず、個人情報は特定されません。
調査期間
調査対象期間:2017年9月1日~2018年8月31日
研究成果の発表
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
糖尿病・内分泌内科 西川武志
当院における研究責任者
糖尿病・内分泌内科 西川武志
問い合わせ先
糖尿病・内分泌内科 西川武志
TEL: 096-353-6501
27. overt diabetes in pregnancy(妊娠中の明らかな糖尿病)の臨床像に関する後ろ向き解析
研究の概要
糖尿病人口の増加、晩婚化とともに、妊娠中に初めて耐糖能低下を指摘される頻度は増加しています。2008年に発表された妊娠中の耐糖尿検査と母児予後に関する大規模観察研究結果(HAPO study)に基づき、2010年に妊娠中の糖代謝に関する診断基準が変更となり、妊娠中に発症もしくは初めて発見された耐糖能低下は妊娠中に初めて発見または発症した糖尿病に至っていない糖代謝異常である妊娠糖尿病(GDM)と妊娠中の明らかな糖尿病(overt diabetes in pregnancy)に分けて定義されました。GDMは、周産期合併症発症を予防するため、妊娠中の厳格な管理が必要となるだけでなく、将来の2型糖尿病のハイリスク群といわれていますが、overt diabetes in pregnancyは妊娠前からすでに耐糖能異常がある症例や妊娠中に糖代謝が悪化した症例、妊娠中に1型糖尿病を発症した症例が含まれ、妊娠中に慢性合併症がすでに存在したり、悪化したり、周産期合併症が起こりやすく、産後のフォローがより大切であるなど妊娠糖尿病以上に妊娠中や産後の管理が重要となります。しかしながら、overt diabetes in pregnancyは、妊娠糖尿病に比し、症例数が限られており、学会主導の前向き調査は進行中ですが、旧診断基準での限られた施設からの報告しかなく、臨床像についての詳細は十分判明していません。
今回当院、糖尿病内分泌内科では、当院に受診歴のある妊娠糖尿病の患者さんのカルテのデータを解析し、後ろ向き解析を行います。なお、研究に関係する全ての医師は、厚生労働省の示している「臨床研究に関する倫理指針」に従って本研究を実施します。また、いかなる場合においても、研究に参加した患者の氏名、住所などプライバシーに関わる事項は一切公表しません。
研究の目的と方法
通常診療より得られる下記のデータを抽出します。
患者の臨床情報、糖代謝指標、インスリン使用の有無
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に取り扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。
本研究にご自身の臨床データを研究に使わないで欲しいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
当院に受診歴のある妊娠糖尿病の患者さんのカルテの臨床データ
調査期間
研究機関:2018年8月30日~2020年3月31日(調査対象期間:2014年1月~2017年12月)
研究成果の発表
学会、論文などでの発表を予定しています。
研究代表者
糖尿病・内分泌内科 小野 恵子
当院における研究責任者
糖尿病・内分泌内科 西川武志、橋本章子、木下博之、大久保侑馬
問い合わせ先
糖尿病・内分泌内科 小野恵子
TEL: 096-353-6501
26. 移植エリア内から移植エリア外へ移動する患者への継続看護を通しての関わり~チェックリストの作成と移動前の関わりを見直して~
研究の概要
6南病棟では年間約50例の移植を行っている。50床の病室のうち個室15床は二重扉でしきられた無菌区域内にある。廊下も含め無菌室レベルを満たしており、移植エリアと呼んでいる。移植を受ける患者は移植前処置から生着後GVHD等の症状が落ち着くまでの間、移植エリア内で最短で1ヶ月程度治療を行い、移植エリア外へ移動となる。6南病棟では固定チームナーシングを行っていることもあり、移植エリア外への移動の際に受け持ち看護師が変更となる。現在の受け持ち看護師変更の際は主に口頭で患者の経過を申し送っている。移植エリア内から移動となるタイミングは、部屋の空き状況、主治医の判断によって左右されるため、急に部屋移動が決まる事もある。そのため、移植エリア外への移動後に受け持ち看護師の変更を行っており、タイムリーに申し送りができていない現状にある。また、受け持ち看護師間で申し送りが不十分であることから、新たな移植エリア外の受け持ち看護師は移植後患者とのコミュニケーションがスムーズに図れず、コミュニケーションに困難さを感じたり、継続した看護が十分に行えていない状況にある。入院途中から受け持つことになるため、患者との関わりや責任感が希薄となったり、受け持ちとしての意識が低くなる、といった傾向がある。患者自身もまた、入院生活が長期化している中で移植エリア外へ移動することになるため、受け持つ看護師や環境の変化が生じることによりストレスを感じやすい状態にある。あまり担当したことのない移植エリア外の看護師へ自分の思いが表出出来ていなかったり、移植エリア未経験の看護師もいるためGVHD症状出現時に症状に対しての具体的な移植の経過の説明不足など、移植エリア内にいたときと比較しての患者からの不満が聞かれることもあった。
大場らは、「患者の向かうべき最善の方向性を看護師の持つ専門的知識を加えながら、共にあゆんでいくことが理想的な患者看護師関係を形成させる要因であり、プライマリー看護師の重要性を示唆している。」と述べており、移植エリア内から移植エリア外へ移動する際の受け持ち看護師の関わり方の見直しを行うことにより患者の精神的苦痛の軽減ができ、患者とのコミュニケーションをスムーズに図れるのではないかと考えた。さらに、受け持ち看護師を中心としてチームで情報を共有することで、身体面・精神面の看護ケアも含めた継続的な看護実践を行うことが看護の質の向上につながると考えた。
研究の目的と方法
目的:病棟カンファレンスを行い、当病棟における移植患者の受け持ち変更前後のフローチャートと移植エリア内から移植エリア外へ移動する際のチェックリストを作成し、看護体制を見直すことで継続看護に繋がることを明らかにしたい。
方法:移植後患者の受け持ち変更時のチェックリスト・フローチャートを作成。スタッフへ周知し取り組みを開始後、取り組み後の体制について継続看護の評価を行う。
本研究の参加について
対象者に対して研究の主旨、方法並びに研究協力による利益・不利益、協力は自由意志であること、撤回の自由を口頭と文書で説明し、文書で同意を得る。得られた内容は個人が特定されることなく研究者以外に漏れることはないこと、また結果を発表する意図があることを文書にて誓約する。研究による看護師に対する心理面への影響を考慮し疑問や不安にはいつでも応じることを明記する。
調査する内容
- 病棟カンファレンスを通して当病棟における移植患者の受け持ち変更前後のフローチャートと移植エリア内から移植エリア外へ移動する際のチェックリストを作成し実践後の看護師としての意識の変化
- 取り組み後の体制について継続看護の評価
調査期間
研究期間:国立病院機構熊本医療センター倫理審査承認後から~平成31年3月
研究成果の発表
本研究は2月の熊本医療センター病院全体での発表を予定
研究代表者
6南看護師 益永千穂
当院における研究責任者
6南看護師 益永千穂
問い合わせ先
6南病棟看護師 益永千穂、大寺真未
25. 急性硬膜下血腫に対する穿頭血腫除去術の有用性について
研究の概要
2009年1月以降に当院にて急性硬膜下血腫に対して穿頭血腫除去術を行った患者様と開頭血腫除去術を行った患者様の経過を比較する研究です。
研究の目的と方法
私たちは急性硬膜下血腫の患者様の来院時の状態、術後経過についてデータを集め、開頭血腫除去術に対する穿頭血腫除去術の非劣性を検証します。
それにより急性硬膜下血腫に対しての手術の選択肢について提言します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆さまの貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
急性硬膜下血腫と診断された患者様の年齢・性別・入院時の意識の状態・画像所見・入院期間・退院時の意識状態と全身状態について、既存のカルテ情報から調査します。患者様の個人情報につきましては記載いたしません。
調査期間
調査対象期間:2009年1月1日~2017年8月31日
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。個人が特定されることはありません。
研究代表者及び責任者
脳神経外科 松浦任
問い合わせ先
脳神経外科 松浦任
TEL: 096-353-6501
24. 診療放射線技師の読影補助能力向上を目的とした国立病院機構九州グループ内における臨床画像アーカイブの作成
研究の目的と方法
厚生労働省の通知より「医療スタッフの協働・連携によるチーム医療の推進について」の中で診療放射線技師は画像検査等における読影の補助を行うようにとされています。この読影とは放射線診断医師がCT検査やMRI検査等の画像から得られた情報を詳細に検査を依頼した各診療科医師に伝えることで、何百枚にもなる画像を見ながらの作業となるため非常に時間と労力を要するものです。今回、この作業の補助を行うにあたってより分かりやすい画像の提供をすることが最善の策と考え、そのためには画像を撮影する診療放射線技師がより精度の高い検査を行う事や病気の特徴的な画像を把握することが必要不可欠です。
診療放射線技師が読影の補助を行うにあたり、必要な知識を集約した手引書を作成することを目的とします。
平成23年から長崎医療センターで行われた研修を基にまとめられた臨床画像セミナー症例集から既定フォーマットを作成し、各共同研究機関(熊本医療センター、九州医療センター、九州がんセンター、嬉野医療センター、鹿児島医療センター)における救急撮影時に多い症例について臨床画像を用い、既定フォーマットに沿って内容をまとめます。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に行います。本研究にご自身のデータの使用をご希望されない方は、あるいはご質問等おありの方は、末尾の問合せ先までご連絡ください。
調査する内容
本研究は、新たな検査をすることはなく、既存カルテ情報のみを用いて実施する研究です。急性胆のう炎・精巣捻転・子宮外妊娠・心筋梗塞・頭部外傷・胸腹部外傷・びまん性軸索損傷・顔面外傷・頸椎損傷の典型的な画像所見を呈する症例のCT検査、MRI検査の内容を調査します。個人情報の取り扱いについては、「人を対象とする医学系研究に関する倫理指針」、「個人情報の保護に関する法律」及び適応される法令、条例等を遵守します。研究対象者の情報を取り扱う場合は秘密保護に十分配慮し、特定の個人を識別することができないようにします。
調査期間
研究期間:倫理審査委員会承認日~西暦2020年3月31日
(調査対象期間:西暦2005年1月~2020年3月)
研究代表者
長崎医療センター診療放射線部主任診療放射線技師 岡原継太
当院における研究責任者
診療放射線科 深松昌博
問い合わせ先
診療放射線科 深松昌博
TEL: 096-353-6501(内線5841)
23. 不明熱診療状況の検討
研究の概要
不明熱は、日常診療で遭遇することが多い病態ですが、診断・治療の明確な指針はなく、診療に苦慮することが多いです。今回、当院を受診された不明熱患者に関して調査を行い、現状把握と問題点を抽出することで、これからの不明熱診療をより向上させることを目的とし、観察研究を計画しました。
研究の目的と方法
本研究では、2015年4月1日~2016年3月31日に国立病院機構熊本医療センターを受診された18歳以上の患者様のうち、①病名・診療録に「不明熱」の記載があり、②「古典的不明熱」の基準を満たしている方を対象としています。日常診療で得られた臨床データ(年齢、性別、検査内容、検査値、最終診断、治療状況、転帰)を電子カルテから集計いたします。
本研究の参加について
これにより患者様に新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。ご自身のデータを本研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
日常診療で得られた臨床データ(年齢、性別、検査内容、検査値、最終診断、治療状況、転帰)を電子カルテから集計いたします。
調査期間
研究期間:2018年7月1日~2018年8月31日(調査対象期間:2015年4月1日~2016年3月31日)
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
総合診療科 辻 隆宏
当院における研究責任者
総合診療科 辻 隆宏
問い合わせ先
総合診療科 辻 隆宏
TEL: 096-353-6501
22. 前立腺癌に対するIMRTにおける下肢固定具の検討
研究の概要
IMRT (強度変調放射線治療)は、従来の放射線治療に比べ、腫瘍の形に合わせて放射線を照射することが可能であり、前立腺の周囲にある臓器(直腸や膀胱)への照射を限りなく少なくすることができる治療法です。このIMRTの精度を高めるには、患者さんの下肢を固定する固定具の再現性が重要になります。
研究の目的と方法
今回の研究の目的は、当院でIMRTを導入するにあたり、全治療期間を通して患者さんの位置セットアップ精度維持のため、下肢固定具の再現性の評価を行うことです。
研究方法は、2017年4月〜2018年5月までの間で、下肢固定具を使用して放射線治療を行なった方の、画像誘導放射線治療の結果を解析し、固定具の再現性の評価を行います。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存の画像誘導放射線治療の画像のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、個人情報は特定されません。
調査期間
研究期間:2017年4月1日~2018年5月31日
研究成果の発表
2018年11月10日〜11日に沖縄で開催される、第13回九州放射線医療技術学術大会で研究発表する予定です。
研究代表者
放射線科 竹口明宏
当院における研究責任者
放射線科 竹口明宏
問い合わせ先
放射線科 竹口明宏
TEL: 096-353-6501
21. 熊本大学脳神経外科関連施設および協力施設における脳腫瘍の疫学調査
研究の概要
本研究は、新たに試料・情報を取得することなく、既存カルテ情報のみを用いて実施する研究です。 脳腫瘍の発生率は人種や地域によって異なるとの報告がありますが、日本での脳腫瘍の疫学調査は散見される程度です。熊本大学脳神経外科関連施設および協力施設が共同し、現在まで熊本県脳腫瘍の発生率を調査する研究を25年以上も続け、その成果は、中枢神経原発胚細胞腫において欧米より日本では、発生率が高いとするなど報告してきました。今後も疫学調査を続け、脳腫瘍の発生と環境要因の関連性などを見いだせれば、何らかの予防医学につながるものと期待しています。
研究の目的と方法
研究デザイン
前向き研究
サンプル
熊本県およびその周辺地域にて発症したすべての脳腫瘍患者を対象とします。患者から侵襲的に得るサンプルはなく疫学的な情報のみ収集します。当院の対象者数は年間20~30人と予測され、今後当院で入院・通院した脳腫瘍患者、および2017年以前の過去症例も対象となります。過去症例については匿名化された情報のみ研究利用されます。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に行います。本研究にご自身のデータの使用をご希望されない方は、あるいはご質問等おありの方は、末尾の問合せ先までご連絡ください。
本研究の参加について
患者さんの個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。登録する内容は次の通りです。
診断名、診断年、年齢、性別、脳腫瘍発症時のKPS(Karnofsky performance Status)、腫瘍摘出の有無、症候性の有無、生存期間、転移性であれば原発巣。
調査期間
2018年7月1日 ~2035 年3月 31日
研究成果の発表
調査した患者さんのデータは集団として分析され、学会や論文で発表される機会があります。しかし、個人が特定されることはありません。
研究代表者
熊本大学大学院生命科学研究部脳神経外科 武笠晃丈
当院における研究責任者
脳神経外科 大塚忠弘
問い合わせ先
脳神経外科 大塚忠弘
TEL: 096-353-6501
20. 腎臓疾患および体液制御の異常に関わる危険遺伝子および遺伝子変異の同定
研究の概要
腎臓は生体の体液の恒常性を制御するも重要な臓器である。そこでは生体が刻々と変化する外界の 状態に対応して、内部環境を一定に保つべく獲得した精巧な機構が存在する。このことは外界からの 刺激からの種々のシグナル伝達を経て、終効果器の腎臓内の様々な輸送体タンパクの機能を調節するという形で達成される。近年、次世代シークエンサーの登場も相まって多くの腎臓疾患および体液 制御異常症(偽性低アルドステロン症 II 型、Liddle 症候群、Gitelman 症候群、Bartter症候群など)の原因となる遺伝子異常が報告され、確定診断、治療予後判定という観点からも遺伝子診断の必要性はさらに高まっている。一方で、原因遺伝子変異が細胞内でいかにしてシグナル受容と機能発現を効果的に行っているかについては未解明の部分が多い。そこで、疾患患者解析により明らかになった変異に焦点をあて、分子変異がもたらす病態メカニズムを把握することが必要となる。
研究の目的と方法
この研究では疾患起因性変異タンパクの解析を通して各種腎疾患における病態メカニズムを解明し、新たな治療戦略を探求することを研究テーマとしている。本研究では、遺伝子変異もしくは遺伝子多型が発症の危険因子になっていると考えられる腎臓疾患および体液制御の異常について、患者検体から危険遺伝子を決定、その配列を明らかにすることを目的としている。患者から 10mL の血液を採取し、DNAを抽出、次世代シークエンサー及びサンガーシークエンス法を用いて遺伝子塩基配列を決定する。対象とするのは、以下に列記する各種腎疾患責任遺伝子およびその関連遺伝子であるが、予想される変異が発見されない場合、国立遺伝学研究所などと共同で網羅的遺伝子解析による新規原因遺伝子発見を目指す。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
血液、10mL シリンジにて採取
調査期間
研究期間:東京医科歯科大学医学部遺伝子解析研究に関する倫理審査委員会承認後〜平成 34 年 3 月 31 日
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表する可能性があります。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
東京医科歯科大学医学部付属病院腎臓内科学教授 内田信一
当院における研究責任者
腎臓内科 中村朋文
問い合わせ先
腎臓内科 中村朋文
TEL: 096-353-6501
19. 当院における誤嚥性肺炎の現状
研究の概要
近年の高齢化に伴い、高齢者の救急搬送件数は増加の一途をたどっていますが、その中でも誤嚥性肺炎が占める割合は小さくありません。今回、当救命救急センターに救急搬送された誤嚥性肺炎患者に関し調査を行い、現状の把握と問題点を抽出することで、これからの肺炎治療をより向上させることを目的とし、観察研究を計画しました。
研究の方法
本研究では、2017年7月1日から2017年12月31日までの半年間に、国立病院機構熊本医療センター 救急外来に受診された15歳以上の患者様のうち、肺炎の診断で入院となった方を対象としています。日常診療で得られた臨床データ(年齢、性別、肺炎分類、重症度、入院診療科、病棟、使用抗生剤、施行した検査、合併症、入院期間など)を電子カルテから集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究で扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
調査対象期間:2017年7月1日~2017年12月31日
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
救命救急科 北田真己
当院における研究責任者
救命救急科 北田真己
問い合わせ先
救命救急科 北田真己
TEL: 096-353-6501
18. 施設におけるAi検査の実際:救急CPA
研究の概要と目的
当院は患者の死因究明のために死後画像検査(Ai)を施行しています。様々な状態におけるご遺体のAiを施行しており、その件数は毎年100件を超えます。改行 研究会において当院におけるAi-CTの撮影時に注意すべき点、死後画像の特徴を報告することにより、Ai件数の少ない他施設の参考になり正確な読影能力の習得を目的とします。
研究の方法
当院におけるAi施行までの流れ、CT撮影方法、注意すべき点を説明します。さらに過去Ai-CTを施行した臨床画像より死後変化、心肺蘇生術後変化、死因の特徴が現れている患者症例について報告します。
本研究の参加について
過去Ai-CT検査を施行した、患者画像(10例程度)およびその患者の生存時のCT画像を使用します。新たな検査や費用の負担が生じることはありません。使用するCT画像は個人が特定されない形で厳重に扱います。使用する患者画像は故人のものになりますので、故人の画像を使わないで欲しいと希望されるご家族の方は末尾の問い合わせ先までご連絡下さい。
調査する内容
過去Ai-CT検査を施行した、患者画像およびその患者の生存時のCT画像のみを使用します。患者ID・氏名・生年月日・検査日等の個人情報は、一切記載せず画像のみを使用するため個人情報は特定されません。
調査期間
研究期間:2012年1月1日~2018年4月1日
研究成果の発表
2018年5月26日に国立病院機構九州医療センターで開催される、九州国立病院機構診療放射線技師会第4回CTセミナーにて施設紹介として報告します。
研究代表者
放射線科 竹尾晃一
当院における研究責任者
放射線科 竹尾晃一
問い合わせ先
放射線科 竹尾晃一
TEL: 096-353-6501
17. 去勢抵抗性前立腺がんに対するドセタキセル療法にペグフィルグラスチムが及ぼす影響
研究の概要と目的
がん化学療法に伴う発熱性好中球減少症は、入院期間の延長や死亡の原因となる重篤な副作用の一つです。この発熱性好中球減少症を予防する目的で本邦では、ペグフィルグラスチム(商品名:ジーラスタ®皮下注3.6 mg)が市販されています。しかしながら、すべての抗がん剤治療に使用されるわけではなく、特に発熱性好中球減少症の発症リスクの高い治療法での使用が推奨されています。去勢抵抗性前立腺がんに対するドセタキセル療法は、発熱性好中球減少症に対して注意が必要な薬剤ですが、現在のところペグフィルグラスチムの積極的な予防投与は推奨されていません。そこで今回当院で去勢抵抗性前立腺がんに対するドセタキセ療法を実施されている患者様を対象に、発熱性好中球減少症の発症頻度を調査し、ペグフィルグラスチムの必要性と有効性を電子カルテより調査いたします。またペグフィルグラスチムは、高価な薬剤であるため医療経済に対する影響も併せて調査いたします。
研究の目的と方法
本研究では、2013年1月から2017年10月の期間に去勢抵抗性前立腺がんに対してドセタキセルが投与された患者様を対象としています。日常診療で得られた臨床データ(年齢、性別、主病名、既往歴、検査結果など)を電子カルテから集計します。また医療費については医事会計システムより算出します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査期間
2018年5月から2019年4月にかけて、カルテを調査します。
研究成果の発表
調査した患者様のデータは、集団として分析し、学会や論文で発表します。また、個々の患者様のデータを発表するときも、個人が特定されることはありません。
研究代表者
治験センター 髙武嘉道
当院における研究責任者
治験センター 髙武嘉道
問い合わせ先
治験センター 髙武嘉道
TEL: 096-353-6501
16. 「有痛性腫瘍病変への放射線治療における調査用紙を用いた有効性評価」のデータを用いた二次解析
研究の概要
痛みのある腫瘍への放射線治療により、痛みをやわらげる効果が期待できます。しかし、どのような患者様に放射線治療が効きやすいかについて、今のところまだ十分には分かっていません。患者様が受けられた放射線治療について研究を行い、痛みの強さ、痛みが生活に及ぼす影響を調べます。
研究の目的と方法
3施設(熊本大学医学部附属病院、熊本医療センター、人吉医療センター)で施行された、前向き観察研究である「有痛性腫瘍病変への放射線治療における調査用紙を用いた有効性評価」のデータを用いた二次解析を行います。すでに得られている情報に加え、患者背景、検査値、治療内容等のデータを新たにカルテより取得します。
本研究の参加について
「有痛性腫瘍病変への放射線治療における調査用紙を用いた有効性評価」に参加された患者様が研究対象者として選ばれました。本研究は既存のデータに基づいた遡及的研究であるため、研究に参加することで、患者様に健康上の危険や有害事象が増えることはありません。
また、いつでも参加の同意を取り消すことができ、それを理由に患者様が不利益を受けることは一切ありません。すでに提供いただいた情報の研究への利用もいつでも中止可能ですので、そのようなご希望があれば末尾の問い合わせ先までご連絡ください。
調査する内容
- 疾患・患者背景・痛みの特徴・治療因子・検査値等ごとの治療効果の評価、比較
- 放射線治療対象病変以外の有痛性病変の解析
- 適切な痛みの評価法
- Pain Management Index(鎮痛薬の使用の妥当性を評価する指標)に関する解析
- 生存に関する解析
- 一時点の痛みの強さ、機能干渉、患者背景等に関する検討
調査期間
研究期間:2018年4月17日~2038年12月31日
研究成果の発表
本研究の結果は、将来の患者の診療に役立てることを目指すもので、研究成果は論文、学会発表として公表します。
研究代表者
熊本大学大学院生命科学研究部放射線治療医学分野教授 大屋夏生
当院における研究責任者
放射線治療科 冨高悦司
問い合わせ先
熊本大学医学部附属病院放射線治療科 斉藤哲雄
TEL: 096-373-5261
15. 一般社団法人日本脳神経外科学会データベース研究事業(Japan Neurosurgical Database:JND)
研究の概要
日本脳神経外科学会会員が所属する日本全国の脳神経外科施設で、学会独自のデータベース、Japan Neurosurgical Database(JND)へ入院患者さんの医療情報を登録します。手術だけでなく検査や読影、内科治療といった非手術症例の登録も含め、日本の脳神経外科領域における診療内容のより正確な実態把握および専門医制度と強く連携したデータベースを構築します。
研究の目的と方法
医療の質の向上に役立て、患者さんに最善の医療を提供することを目指します。医療情報はインターネットを介して登録され、収集したデータを分析することで日本の脳神経外科領域における以下の点について明らかにします。
- 手術を含む脳神経外科医療を行っている施設の特徴
- 医療水準の評価
- 手術・治療を受けた方の予後
- これから手術を受ける方の死亡・合併症の危険性の予測など
- 専門医の更新要件到達度
- 専攻医の研修目標到達度
- 脳神経外科専門医制度のあり方に関する基礎資料
- 医療機器や薬剤などの市場調査
- 臨床研究、治験などを計画する際の基礎資料
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に行います。本研究にご自身のデータの使用をご希望されない方は、あるいはご質問等おありの方は、末尾の問合せ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することなく、既存カルテ情報のみを用いて実施する研究です。患者さんの個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。登録する内容は次の通りです。
「性別、生年月(日は除外)、年齢、居住地の郵便番号(上3桁のみ)、発症日、主治医情報、発症時症状、入院日、主病名、治療内容(手術、診断検査、教育入院、内科治療、化学療法、放射線治療、リハビリ、終末期管理)、退院日、退院先、退院時状況、担当医、術者情報」
調査期間
研究期間:2018年1月1日から2023年9月30日
研究成果の発表
調査した患者さんのデータは集団として分析され、学会や論文で発表される機会があります。しかし、個人が特定されることはありません。
研究代表者
山形大学医学部先進医学講座 嘉山孝正
一般社団法人日本脳神経外科学会理事長 新井一
当院における研究責任者
脳神経外科 大塚忠弘
問い合わせ先
脳神経外科 大塚忠弘
TEL: 096-353-6501
14. 薬剤血管外漏出に対するステロイド局注、及びそのクリティカルパスの有効性と問題点の検討
研究の概要
従来より血管内に注射しようとした薬剤(とくに抗がん剤)が血管の外に漏れる「血管外漏出」が起きたときは、炎症を抑えるステロイドを局所に注射することが有効であると言われ、治療に使われていました。一方で十分な科学的根拠がなく、反対意見も少なくありませんでした。そして最近、一部の抗がん剤が漏れたとき専用の治療薬も発売されました。また当院では患者様の救命のために必要であるが、血管から漏れると皮膚が損傷しやすい薬剤の使用頻度が多く、その血管外漏出対策は重要な課題でした。
2012年10月から当院では「血管外漏出クリティカルパス」を作成し、薬剤が漏れた部位にステロイド、局所麻酔薬などを速やかに注射し、ステロイド軟膏と湿布を行いながら経過を見るという一連の手順を一括指示できるようにしました。また先述の抗がん剤血管外漏出治療薬が保険適応になったのに伴い、改訂も行ないました。パスの運用を開始して丸5年が経過したので、その有効性や問題点を再検討する観察研究を行い、今後の治療の質の改善に役立てたいと思います。
研究の目的と方法
本研究では、2012年11月から2017年10月末までの5年間、国立病院機構熊本医療センターにて薬剤の血管外漏出について診察を受けられた方を、入院・外来を問わず対象としています。日常診療で得られた臨床データ(年齢、性別、主病名、既往歴、検査結果など)を電子カルテから集計します。また皮膚症状の臨床写真を撮影している場合にはそれも参考にします。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
2018年2月から2020年3月にかけて、カルテを調査します。
研究成果の発表
調査した患者さんのデータは、集団として分析し、2018年5月31日~6月3日に広島市で開催される第117回日本皮膚科学会総会にて一般演題として発表します。その後、論文して皮膚科関連学術雑誌に投稿する予定です。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
皮膚科 牧野公治
当院における研究責任者
皮膚科 牧野公治
問い合わせ先
皮膚科 牧野公治
TEL: 096-353-6501
13. 蜂巣炎における圧迫療法併用の有用性について
研究の概要と目的
下肢の皮膚細菌感染症「蜂巣炎」では、足から心臓に戻る血流がとどこおる「下肢静脈うっ滞」がリスク因子の1つであることが知られています。その重要の治療法の1つに包帯やサポーターで下肢を圧迫する「圧迫療法」があります。以前は蜂巣炎を起こしている時は圧迫療法を行っていませんでしたが、リンパの流れの滞りから細菌感染が血管に及ぶことや血流に問題があると局所の抵抗力が下がることが報告されており、むしろ細菌感染の悪化防止につながるのではないかと考えられます。そこで蜂巣炎における圧迫療法の有用性を検討するため、観察研究を計画しました。
研究の方法
本研究では、2011年4月から2016年3月末までの5年間、国立病院機構熊本医療センター皮膚科に皮膚細菌感染症の治療のため入院した方を対象としています。日常診療で得られた臨床データ(年齢、性別、最終診断名、既往歴、バイタルサイン、血液検査結果、画像検査結果、使用した抗菌薬、入院期間など)を電子カルテから集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆様の貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究にご自身のデータを研究に使わないでほしいと希望されている方、その他研究に関してご質問がございます際は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
調査期間
2018年2月から2020年3月にかけて、カルテを調査します。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究成果の発表
皮膚科 牧野公治
当院における研究責任者
皮膚科 牧野公治
問い合わせ先
皮膚科 牧野公治
TEL: 096-353-6501
12. 悪性腫瘍と動脈硬化疾患との併存に関する調査
研究の目的
日本人の三大死因は悪性腫瘍、心疾患、脳血管疾患であり、高齢化社会の進展に伴い、それらの疾患群を診療する機会は増加する傾向にあります。動脈硬化性疾患と悪性腫瘍は相対立するものではなく併存していることもよく見られ、複雑疾患の多い大学病院では特にその傾向が強く治療の優先順位に苦慮することがあります。しかしながら現時点において悪性腫瘍と動脈硬化疾患との関連についてはその併存率や関連などについては十分解明されていない。今回当院において動脈硬化を扱う診療科ならびに悪性腫瘍を扱う診療科にてこれらを調べることで、今後の診療の助けになることが期待できます。
今回の研究で国立病院機構熊本医療センター循環器内科にご入院された全ての患者様を対象とします。本研究で得られる情報は、本研究のみに用いられます。
利用する試料・情報
平成29年10月1日~平成29年12月31日までの年齢・性別・基礎疾患・入院歴・服薬歴・血液検査・心電図・心エコー・心臓カテーテル検査から得られる情報。
※個人が特定できる情報や、ID番号は研究には利用しません。研究データ上にも残りませんので、本研究から個人情報が流出することは基本的にありません。また、研究の成果を公表するときにおいても個人情報が漏出する可能性は極めて低く、患者様に危険や不利益が生じることはありません。
研究実施施設及び責任者
研究実施機関の名称:熊本医療センター循環器内科
研究担当者:藤本和輝
研究への利用を停止する場合
患者様においては、得られた情報の研究への利用をいつでも停止することができます。研究に不参加となった場合も、患者様に不利益が生じることはありません。申し出をされる場合は本人又は代理人の方より、下記の連絡先までお問い合わせください。
研究実施期間
倫理員会承認の日から平成29年12月31日まで
連絡先
研究利用の停止、そのほか質問したいことなどがありましたら、下記の担当者までご連絡ください。
国立病院機構熊本医療センター
〒 860-0008 熊本県熊本市中央区二の丸1-5
連絡先:096-353-6501
担当医師:藤本和輝
11. 2Dトラッキングを利用したPPP仮想透視画像作成の検討
研究の概要
本研究は、平成29年4月に新たに導入された血管造影装置を用いた研究です。この装置は、CTのボリュームデータから作成したIVR手技支援画像とCアーム回転角度連携、テーブル位置連携が可能です。近年の救急IVRでは、これら機能を利用するPPP(pre-procedural planning)が活用され、より確実で迅速なIVR手技が行われています。そこで、造影CTのデータを使用し、いかに迅速かつ正確にPPPを活用できるかを検討しています。
研究の目的
当院では、目的血管までの血管走行トレースラインを表示するPPP仮想透視画像を作成しています。本研究では、ワークステーション装置の2Dトラッキング機能を利用して、より迅速かつ正確に作成することを目的とします。平成26年9月~平成29年4月までに撮影された造影CTのデータを無作為に選び、2点プロットでトーレスラインを抽出するワークステーション装置の2Dトラッキング機能を利用し、迅速かつ正確に作成ができるか検討を行います。IVRの穿刺部位の血管から各目的血管を結ぶトレースラインを抽出する時間を計測し、成功率を記録します。この2Dトラッキングが有用であると示唆されれば、緊急IVRにおいてPPP仮想透視画像が選択されることとなります。
本研究への参加について
本事業への参加は、患者さんの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否していただくことができます。その場合は、病院の担当医または下記問合せ先に御連絡ください。なお、登録を拒否されたことで、日常の診療などにおいて患者さんが不利益を被ることは一切ございません。
調査する内容
平成26年9月~平成29年4月までに造影CTを施行された患者様のデータを調査します。患者様の氏名・住所・生年月日など個人を特定する情報は収集しません。
対象となる患者さんの利益・不利益
この研究は、患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。データの解析においても、先にも述べたように、個人情報は調査しないので、個人情報が漏洩する心配はありません。
調査期間
2017年4月から2017年12月にかけて、当院の診療放射線技師がカルテを調査します。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。個人情報は調査しないので、個人が特定されることはありません。
当院の研究責任者
放射線科 尾崎槙哉
問い合わせ先
放射線科 尾崎槙哉
TEL: 096-353-6501
10. 肝硬変患者の予後を含めた実態を把握するための研究
研究の概要
肝疾患患者さんは、病期の進行状況により、慢性肝炎、肝硬変、肝癌に大きく分類されます。肝癌患者さんに関する患者数や予後調査については国内外から多数報告されていますが、肝硬変患者さんを対象とした調査研究は限定的であり、肝硬変患者さんの数、肝硬変の病期の進展状況や生命予後については十分検討されていないのが実情です。一方、2010年から腹水、黄疸など症状のある肝硬変患者さんは身体障害者手帳の受給対象者となり、2016年にはその基準が改訂されました。今後、身体障害者手帳の基準を検討する上でも、わが国の肝硬変患者さんの実態を把握する必要があります。
本研究では、肝疾患患者さんにおける肝硬変患者さんの頻度、慢性肝炎から肝硬変への進展率、肝硬変患者さんの生命予後と肝硬変の病期の進展状況(Child-Pugh分類)などを明らかする為に、日常診療でえられた情報をもとに調査研究をおこないます。
研究の目的と方法
本研究では2つのグループの患者さんを対象として解析をおこないます。
- 2011年1月から12月末までの1年間、国立病院機構36施設に通院、治療中の慢性肝疾患患者さんについて、DPC(Diagnosis Procedure Combination; 診断群分類)を含む診療情報データで患者登録をおこなうグループ。
- 2016年10月から2017年12月までの期間に国立病院機構36施設に加えて国立国際医療研究センターの各施設に通院、治療中の肝硬変患者さんの登録をおこなうグループ。
本研究は日常診療で得られた臨床データ(肝疾患の原因、肝がんの有無、治療の状態、血液検査所見、腹水の有無、食道胃静脈瘤の有無など)を電子カルテから集計します。
本研究の参加について
これにより患者さんに新たな検査や費用の負担が生じることはありません。また、研究に扱う情報は、個人が特定されない形で厳重に扱います。皆さんの貴重な臨床データを使用させていただくことにご理解とご協力をお願いいたします。本研究に関する研究計画書および研究の方法に関する資料を入手又は閲覧されたい場合、もしくはご自身のデータを研究に使わないでほしいと希望されている方、またこの研究に関して質問、相談されたい方は、末尾の問い合わせ先までご連絡ください。
調査する内容
本研究は、新たに試料・情報を取得することはなく、既存カルテ情報のみを用いて実施する研究です。研究対象者(患者さん)の個人情報(氏名、住所、電話番号、カルテ番号など)は記載せず、対応表を作成して管理しますので、個人情報は特定されません。
対象とする患者さんの利益・不利益
本研究は観察研究であり、研究対象者個人への直接的な利益や不利益は生じません。研究の成果は、肝疾患患者、肝硬変患者の診療の進歩に有益となる可能性があります。
調査期間
研究期間:2017年10月17日~2020年3月31日(調査対象期間:2011年1月~2019年12月)
研究成果の発表
研究者は、本研究のAMEDの報告書(2020年3月)にまとめて発表します。また、関連学会(未定)や学術雑誌(未定)において発表を予定しています。
研究代表者
国立病院機構長崎医療センター臨床研究センター 八橋弘
当院における研究責任者
消化器内科 杉和洋
問い合わせ先
消化器内科 杉和洋
TEL: 096-353-6501
9. 胃癌による胃出口狭窄症に対する治療法の実態調査
研究の概要
胃癌により胃の出口をふさがれた患者さんでは、食物が胃から腸に流れることができず、食事をとることができません。このような状態を胃出口狭窄症と言います。胃出口狭窄症の患者さんには、食事が食べれるように胃と腸を縫い合わせて食べ物の出口を新たに造る手術(バイパス手術)と胃カメラで癌によりふさがれた通り道にステントというパイプのような器具を入れて、食べ物の通り道を広げる手術(ステント挿入術)があります。本研究は、日本胃癌学会でデータの登録事業を行っている全国の病院で、2015年1月から2015年12月までに胃癌により胃の出口をふさがれた患者さんでバイパス手術またはステント挿入術を受けた方を対象に、患者さんの状態や検査所見、治療法、合併症、治療効果、予後を調査します。
研究の目的
現在、バイパス手術およびステント術がどのような患者に行われ、どの程度の効果と安全性があるのかよく分かっていない状況です。本研究では、胃癌による胃出口狭窄症の患者さんに行われているこれらの治療の有効性、安全性及び治療予後の実情を把握するとともに、治療成績に影響を与える因子を検討することにあります。これにより、今後同じような症状を持つ患者さんに対して、より安全で効果的な治療が選択されようになり、治療成績の向上が期待されます。
本研究への参加について
本研究への参加は、患者さんの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否して頂くことができます。その場合は、病院の担当医または下記問合せ先にご連絡ください。なお、登録を拒否されたことで、日常の診療等において患者さんが不利益を被ることは一切ございません。
調査する内容
患者さんの年齢や持病の有無・検査データと手術後の状態を調査します。患者さんの氏名・住所・生年月日など個人を特定する情報は収集しません。
対象となる患者さんの利益・不利益
この研究は、患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。また、本研究で得られた病歴や検査所見などの情報は遺漏がないよう十分注意して取り扱います。
調査期間
2017年10月から2018年6月にかけて、参加病院の医師がカルテを調査します。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
岐阜大学医部腫瘍外科 吉田和弘
当院における研究責任者
外科 岩上志郎
問い合わせ先
治験センター 高武嘉道
TEL: 096-353-6501
8. 当院における学童以降の食物アレルギー児の検討
研究の概要
本研究は,2015年1月から2018年12月までに当院を受診された学童以降の鶏卵アレルギーの経過について検討します。
研究の目的
鶏卵アレルギーを主訴に見えるこどもさんの多くについて、経口負荷試験を行うことで、卵をある程度は食べられることが確認できました。これをデータとして示すことで熊本県内ではまだ検査可能施設が少ないため検査を受けることが少し難しい、経口食物負荷試験の普及を訴えることができることを期待しています。
本研究への参加について
本事業への参加は、患者さんの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否していただくことができます。その場合は、病院の担当医または下記問合せ先に御連絡ください。なお、登録を拒否されたことで、日常の診療などにおいて患者さんが不利益を被ることは一切ございません。
調査する内容
食物アレルギーのために当院を受診された患者さんで、鶏卵を除去されていた方が調査対象となります。性別、年齢、発症時期、合併症(喘息、アトピー性皮膚炎)、既往歴(負荷試験、アナフィラキシー)、身体所見、血液検査データ等を調べます.患者さんの氏名・住所・生年月日など個人を特定する情報は調査しません.データは過去のカルテから調べるだけですので、新たな情報の聴取や採取はありません。
対象となる患者さんの利益・不利益
この研究は、患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。データの解析においても、先にも述べたように、個人情報は調査しないので、個人情報が漏洩する心配はありません。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。個人情報は調査しないので、個人が特定されることはありません。
当院の研究責任者
小児科 緒方美佳
問い合わせ先
小児科 緒方美佳
TEL: 096-353-6501
7. 熊本県防災ヘリのドクターヘリ的運用での現場活動の検討
研究の概要
本研究は、2014年4月から2017年3月までに当院が搭乗医師を派遣した熊本県防災ヘリのドクターヘリ的運用(医師同乗現場派遣)の活動内容について検討する。
研究の目的
熊本県防災ヘリは全国でも有数のドクターヘリ的運用を行っていますが、同じく全国に普及するドクターヘリとは運航体制(待機方法、搭乗人員など)が異なります。防災ヘリのドクターヘリ的活用の現場活動について、ドクターヘリと比較検討し、活動内容を改善していくことが目的となります。
本研究への参加について
本事業への参加は、患者さんの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否していただくことができます.その場合は、病院の担当医または下記問合せ先に御連絡ください。なお、登録を拒否されたことで、日常の診療などにおいて患者さんが不利益を被ることは一切ございません。
調査する内容
熊本県防災ヘリで当院に搬送された患者さんが調査対象となります。救急現場での活動時間経過や治療内容を調査します。患者さんの氏名・住所・生年月日など個人を特定する情報は調査しません。データは過去のカルテから調べるだけですので、新たな情報の聴取や採取はありません。
対象となる患者さんの利益・不利益
この研究は、患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。データの解析においても、先にも述べたように、個人情報は調査しないので、個人情報が漏洩する心配はありません。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。個人情報は調査しないので、個人が特定されることはありません。
当院の研究責任者
救命救急科 金子唯
問い合わせ先
救命救急科 金子唯
TEL: 096-353-6501
6. 妊娠糖尿病の病態解析
研究課題名
妊娠糖尿病の病態解析
―インスリン治療を必要とした妊娠糖尿病患者の予測因子の解析と妊娠糖尿病患者の分娩後の耐糖能についての後ろ向き解析―
研究の概要
妊娠糖尿病は「妊娠中に発症もしくは初めて発見された耐糖能低下(血糖値の上昇)」と定義されています。近年本邦では、女性のライフスタイルの変化に伴い晩婚、晩産化が進んでいます。加えて2010年に妊娠糖尿病の診断基準が変更になり、妊娠糖尿病患者数は約3〜4倍に増加しています。他の医療機関における調査研究によると、その頻度は全妊婦の12.08%になると報告されています。 妊娠糖尿病は、たとえ糖尿病の程度が軽度であっても巨大児など、周産期の様々な合併症のリスクとなります。従って、妊娠糖尿病では厳格な血糖管理が必要です。血糖管理法としては、適切な食事療法が中心となりますが、食事療法で血糖管理目標が達成できない場合には、積極的にインスリン治療を行う必要があります。
一方、妊娠糖尿病と診断された女性は、将来の2型糖尿病発症のハイリスク群でもあります。さらに、一度妊娠糖尿病と診断された女性では次回妊娠時においても妊娠糖尿病を発症する可能性が高いことも知られています。従って、妊娠糖尿病と診断された女性は、産後早期(産後6~12週時)に、糖尿病が改善しているかを調べる検査を受けることが推奨されています。
今回当院、糖尿病内分泌内科では、当院に受診歴のある妊娠糖尿病の患者さんのカルテのデータを解析し、下記の2つの後ろ向き解析を行います。
- 食事療法のみで管理を行えた症例とインスリン治療が必要となった症例を比較検討し、インスリン治療の必要性を予測する因子がないかを調べます。
- 産後に施行した糖負荷試験の結果を解析し、妊娠糖尿病既往女性の非妊娠時の耐糖能について、その特徴を調べます。
なお、研究に関係する全ての医師は、厚生労働省の示している「臨床研究に関する倫理指針」に従って本研究を実施します。また、いかなる場合においても、研究に参加した患者の氏名、住所などプライバシーに関わる事項は一切公表しません。
研究成果については、学会、論文などでの発表を予定しています。
研究代表者
糖尿病・内分泌内科部長 西川武志
共同研究者
糖尿病・内分泌内科医師 小野恵子、橋本章子、木下博之、荒木裕貴
5. 救急外来を受診した自傷・自殺企図関連症例の実態把握と予後調査
研究の概要
本研究は、2009年1月から2014年3月までに当院の救急外来を自傷行為、自殺企図で受診した患者さんを対象に、受診時の状況や症状、検査結果とその後の再自傷の有無を検証します。
*この研究は、2016年3月31日の時点で、共同研究事務局へのデータの送付が完了いたしました。
以後、当院からデータの登録を行うことはありません。ご協力ありがとうございました。
研究の目的
自傷、自殺企図の既往は将来の自殺のリスクであることが知られており、自傷が起こった際に適切な評価と対応をすることがとても大切なことです。今回私たちは、自傷行為、自殺企図で受診した患者さんのデータを調査して、将来の再自傷、自殺の危険兆候は何かを検証します。
本研究への参加について
本事業への参加は、患者さんの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否して頂くことができます。その場合は、病院の担当医または下記問合せ先にご連絡ください。なお、登録を拒否されたことで、日常の診療等において患者さんが不利益を被ることは一切ございません。
調査する内容
患者さんの年齢や受診状況、問診の内容、症状、既往歴、検査データ、治療内容と、退院後の自傷行為の有無を調査します。患者さんの氏名・住所・生年月日など個人を特定する情報は調査しません。データは過去のカルテから調べるだけですので、新たな情報の聴取や採取はありません。
対象となる患者さんの利益・不利益
この研究は、患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。データの解析は慶應義塾大学医学部精神・神経科と東京都医学総合研究所の医師も行いますが、先にも述べたように、個人情報は調査しないので、個人情報が漏洩する心配はありません。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。個人情報は調査しないので、個人が特定されることはありません。
当院の研究責任者
精神科 渡邉健次郎
問い合わせ先
精神科 渡邉健次郎
TEL: 096-353-6501
共同研究者
慶應義塾大学医学部精神・神経科 藤澤大介
共同研究事務局
慶應義塾大学医学部精神・神経科 川原庸子
4. 消化器外科緊急手術症例における術後死亡予測モデルCORES、NSQIPの比較検証試験
研究の概要
本研究は、全国の国立病院15施設で、2014年12月から2017年3月までに、緊急で胃や腸など消化器系の手術を行った患者さんを対象に、手術前の状態から手術後の経過を予測できるシステムを検証する研究です。
研究の目的
消化器系の緊急手術を受ける患者さんは、術後にしばしば腹膜炎や肺炎など重大な合併症を併発することがあります。患者さんの手術前の状態から、手術後の状態(予後)を予測することは、主治医にとってとても大切なことです。緊急手術における予後予測法としては、アメリカで開発されたNSQIPと我が国で開発されたCORESがあります。今回私たちは、消化器系緊急手術を行った患者さんのデータを調査して、この二つの方法を比較検証します。また、これらを用いて病院間の外科技術水準の評価が可能か検討します。
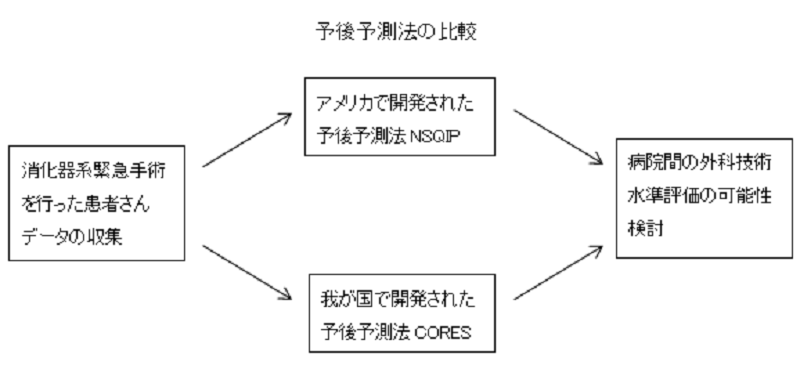
本研究への参加について
本事業への参加は、患者さんの自由な意思に基づくものであり、参加されたくない場合は、データ登録を拒否して頂くことができます。その場合は、病院の担当医または下記問合せ先にご連絡ください。なお、登録を拒否されたことで、日常の診療等において患者さんが不利益を被ることは一切ございません。
調査する内容
患者さんの年齢や持病の有無・検査データと手術後の状態を調査します。患者さんの氏名・住所・生年月日など個人を特定する情報は調査しません。
対象となる患者さんの利益・不利益
この研究は、患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。先にも述べましたが、個人情報は調査しないので、個人情報が漏洩する心配はありません。
調査期間
2014年12月から2017年3月にかけて、参加病院の医師がカルテを調査します。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
臨床研究部 芳賀克夫
当院の研究責任者
外科 宮成信友
問い合わせ先
治験センター 山下克也
電話: 096-353-6501
3. 胃癌切除例の予後調査ESAGC study
研究の概要
ESAGC studyは、全国の病院で、2007年4月から2009年3月までに胃癌にて切除手術を行った患者さんの術後生存期間を調査する研究です。
研究の目的
私たちは胃癌患者さんの年齢や持病の有無・検査データ(お体の状態)、癌の特徴から、手術後5年間生存する割合(5年生存率)を予測することが可能か検証します。同時に、この手法が病院間の医療技術水準の評価に役に立てることができるかを調べます。

調査する内容
患者さんの年齢や持病の有無・検査データ・癌の特徴と手術後の生存期間を調査します。患者さんの氏名・住所・生年月日など個人を特定する情報は調査しません。
対象となる患者さんの利益・不利益
この研究は、すでに手術を行った患者さんのデータをカルテなどから調べるだけですので、対象となる患者さんに利益及び不利益はありません。先にも述べましたが、個人情報は調査しないので、個人情報が漏洩する心配はありません。
調査期間
2014年7月から2015年12月にかけて、参加病院の医師がカルテを調査します。
研究成果の発表
調査した患者さんのデータは、集団として分析し、学会や論文で発表します。また、個々の患者さんのデータを発表するときも、個人が特定されることはありません。
研究代表者
臨床研究部 芳賀克夫
問い合わせ先
治験センター 山下克也
TEL: 096-353-6501
2. 心拍再開した院外心肺停止患者の頭部CTのCT吸収値の調査研究
目的
一時的な心停止の後の意識障害(低酸素性脳症)は、患者様の予後や治療方針に大きな影響を与えます。近年、この低酸素性脳症に対する治療として脳低温治療が推奨され、広く行われるようになりましたが、その適応についてはまだ明らかにされていません。
過去のいくつかの小規模な研究では、心臓の動きが戻った直後の頭のCT検査のCT吸収値(画像の色の濃さ)が予後と関連する可能性を示唆しています。また、本邦における多施設大規模研究では、心臓の動きが戻るまでの時間が短いほど脳低温治療が有効であることが報告されています。
これまで、当院に搬送された心臓の動きが戻った心停止患者様で、頭部CTが撮影された方の病院前情報やその後の治療や予後を調査し、その関係性を明らかにします。
内容
2007年~2012年に当院に来院された心停止患者様のうち、心臓の動きが戻り、その後頭部CTが撮影された方を対象とし、病院前情報(目撃の有無、近くにいる人の胸骨圧迫などの蘇生の有無、発見時刻、救急隊接触時刻、初期心電図、病院到着時刻、心拍再開時刻、心停止の原因)、頭部CTのCT吸収値、心臓が戻った後の治療、機能的予後、生命予後を調査し、これらの関係性について検証します。
研究責任者
救命救急科 原田正公
1. 「独立行政法人国立病院機構における診療情報に係る分析研究」に際する診療情報の研究利用
(独)国立病院機構本部総合研究センター診療情報分析部では、患者様に提供する医療の質の向上を目的として、(独)国立病院機構に属する各病院の診療情報を活用した分析研究を実施することとなりました。
調査対象になるのは患者様の入院・外来の診療情報となります。対象期間は、入院は平成16年7月以降、外来は平成22年4月以降の診療情報となります。
入院患者様の診療情報は、「入院中の診療内容を記載した診療報酬明細書」および厚生労働省が実施している「DPC導入の影響評価に関する調査」に提出しているデータを二次利用させていただくことになります。外来患者様の診療情報については、「外来での診療内容が記載された診療報酬明細書」を二次的に利用させていただくことになります。
具体的には、患者様に提供させていただいた医療行為(処置、検査、処方薬剤)等の内容やその金額に係る情報となります。これらの診療情報は、良質な医療を患者様に提供することを目的として、臨床評価指標を活用した医療の質の評価、診療機能・診療行為に係る分析に活用いたします。
この分析研究の実施にあたり、全て既存の診療情報を活用いたしますので、新たに患者様から情報を収集させていただくことはございません。また、これらの診療情報の活用において、患者様のお名前は匿名化いたしますので、患者様個人が同定されることはなく、またプライバシーに係る個人情報の外部漏洩が起きることも一切ございません。このように、患者様に何らかの負担が生じることはございませんので、ご安心ください。
なお、本分析研究の結果に関しては、国立病院機構内で活用するとともに、患者様・国民の皆様、国立病院機構以外の医療機関に向けて、国立病院機構における医療の質に関する情報開示として公開することがあります。また、医学的な学会での発表や専門的な雑誌で報告することもあります。
この件に関しまして、ご不明な点がございましたら遠慮なく下記窓口までお問い合わせください。
なお、倫理的配慮として、「独立行政法人国立病院機構における診療情報に係る分析研究」に際する診療情報の研究利用に関して、国立病院機構本部のHPで公表をしております。
お問い合わせ先
〒152-8621
東京都目黒区東が丘2-5-21
国立病院機構本部総合研究センター診療情報分析部研究担当者
TEL: 03-2712-5133


