治験(試験)依頼者の方へ
当院に治験等を依頼または依頼予定のある依頼者様は、治験センター(613-Chiken@mail.hosp.go.jp)までご連絡をお願いいたします。
ヒアリング等治験実施の可能性や今後の日程等を決めさせていただきます。
申請等に必要な情報等は以下より入手できます。
ヒアリング等治験実施の可能性や今後の日程等を決めさせていただきます。
申請等に必要な情報等は以下より入手できます。
更新情報
- 2024年10月28日
規定集・様式集・書式:文書番号(5)及び(12)を更新 - 2024年3月22日
院内検査 日本医師会臨床検査精度管理調査参加証を更新
日本臨床衛生検査技師会臨床検査精度管理調査参加証を更新 - 2023年9月13日
治験実績 当院の治験実績:新規課題受託件数(層別)/国際共同治験割合、診療科別契約課題数、対象疾患別治験実績、及び国際共同治験への取り組みに2023年度分を追加し、更新
院内採用検査基準値(2024/2/1)を更新
規定集・様式集・書式
申請にあたっては本ページより必要書式を入手していただき作成をお願いいたします。
※以下の情報は不定期に更新されますので、必ず「再読み込み」を実施後、内容のご確認等をお願いいたします。
※以下の情報は不定期に更新されますので、必ず「再読み込み」を実施後、内容のご確認等をお願いいたします。
| 区分 | 文書番号 | 文書名 | 更新日 |
|---|---|---|---|
| 受託研究取扱規定 | (1) | 国立病院機構熊本医療センター受託研究取扱規定 | 2022/03/16 |
| 医薬品の治験 製造販売後臨床試験 (企業主導) |
(2) | 関係書式取扱について | 2022/03/16 |
| (3) | 標準業務手順書(一式) | 2022/03/16 | |
| (4) | 統一書式(一式) | 2022/03/09 | |
| (5) | 算定要領・契約書 | 2024/10/28 | |
| (6) | 電子媒体取扱規定 | 2013/10/15 | |
| (7) | 治験等に係る書類における押印省略の運用について | 2014/07/07 | |
| (8) | クラウドシステムDDworksNX/Trialsiteの使用について | 2023/02/01 | |
| 医薬品の治験 (医師主導) |
(9) | 統一書式(一式) | 2023/03/09 |
| (10) | 標準業務手順書(一式) | 2022/03/16 | |
| 同意説明文書雛形 | (11) | 治験同意書雛形 ※現在検討中 | 2019/04/04 |
| 製造販売後調査 | (12) | 関係書式一式 | 2024/10/28 |
| 中央治験審査委員会 | (13) | 申請から審査結果通知までの流れ | 2012/04/01 |
| (14) | 熊本医療センター中央治験審査委員会手順書一式 | 2015/04/20 | |
| (15) | 関連書類一式 |
施設選定のための情報
環境整備(設備)
- インターネットの状況:治験センター単独の光回線保有(無線LAN対応)
- 国際電話・FAX:可能(治験センター単独回線保有)
- EDC関連:入力可能。個人用端末の他にEDC入力用端末を完備
- 心電図等のデータ送信:データの海外送信可
- CT・MRI等の電子媒体化のマスキング:可能
- 治験に伴う医療機器の搬入経験:あり(心電図測定機器、スパイロメーター)
人員および体制
現在、薬剤師3名(専任)、看護師4名(専任)、事務員2名(専任)で、治験体制を整え治験の実施に取り組んでいます。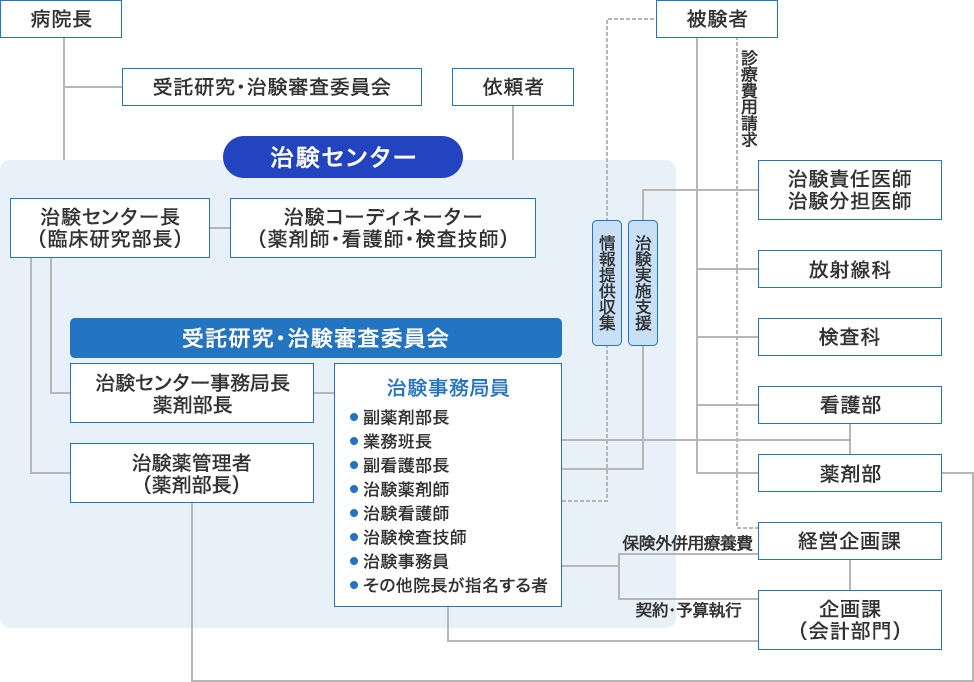
2017/9/7更新
治験実績
当院の治験実績
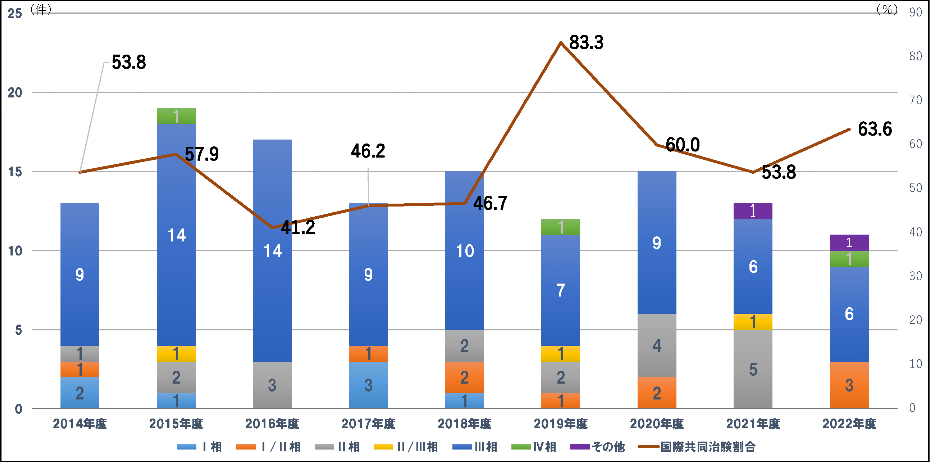
新規課題受託件数(層別)/国際共同治験割合
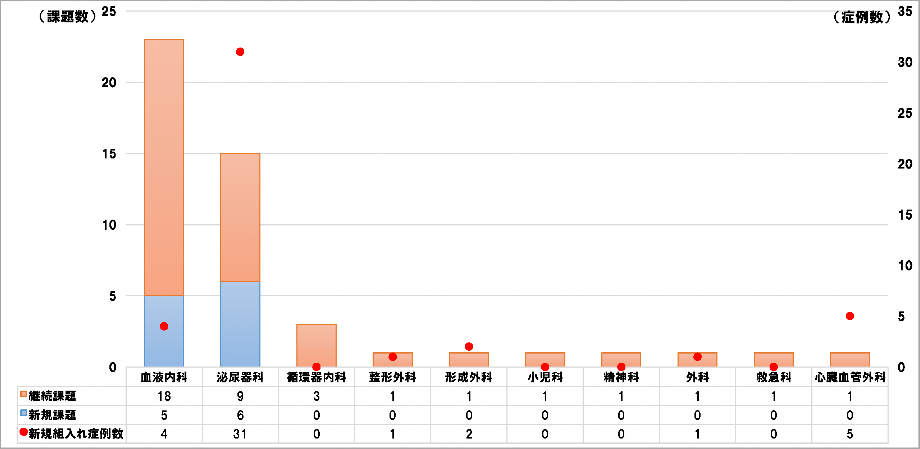
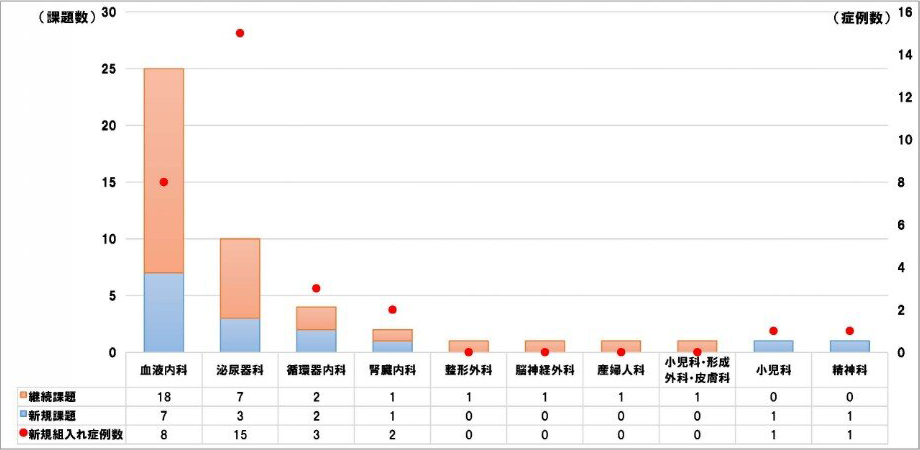
診療科別契約課題数(2023年度分)
診療科別契約課題数(2022年度分)
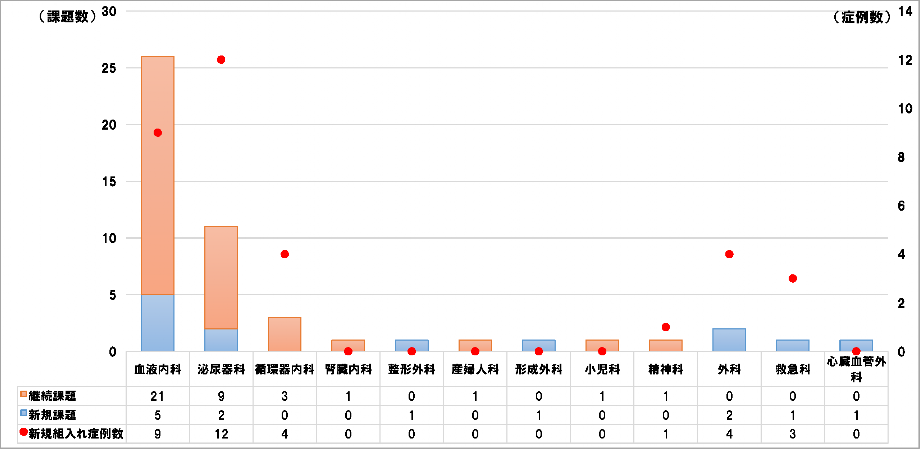
診療科別契約課題数(2021年度分)

診療科別契約課題数(2020年度分)
対象疾患別治験実績
2023年度終了課題
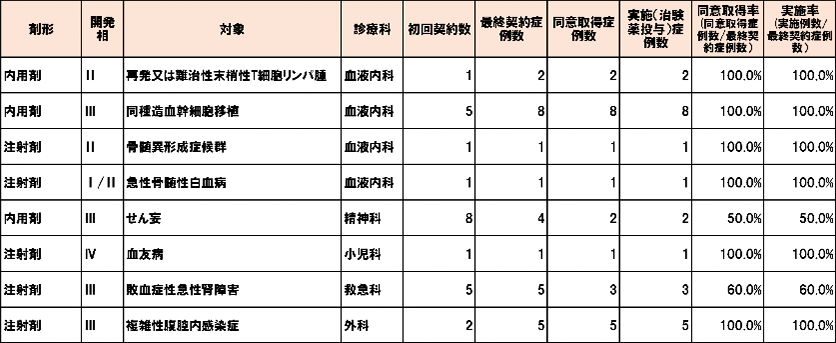
2022年度終了課題

2021年度終了課題 実施率50%以上のみ
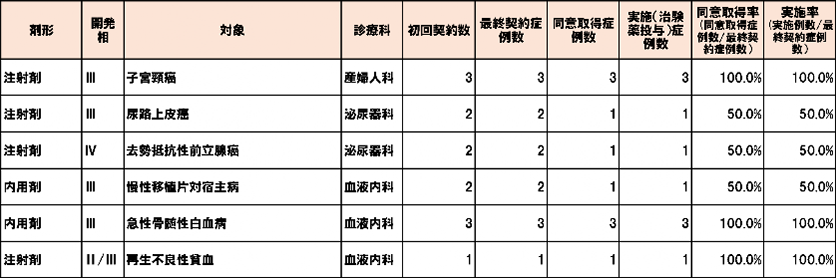
2020年度終了課題 実施率50%以上のみ
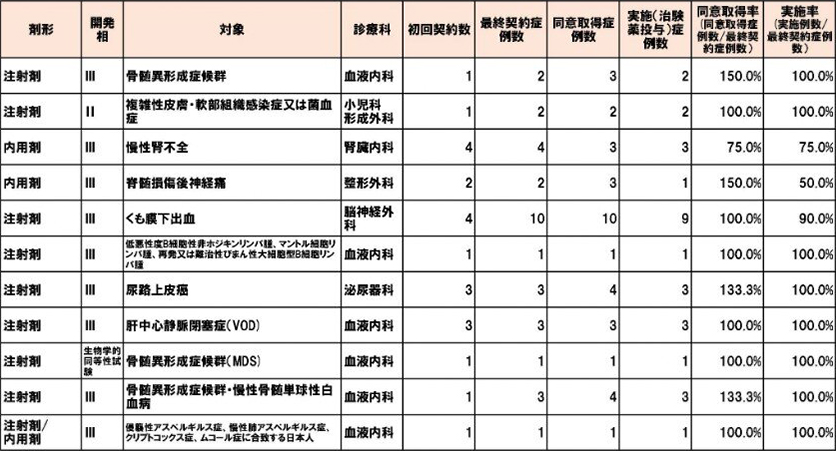
2019年度終了課題
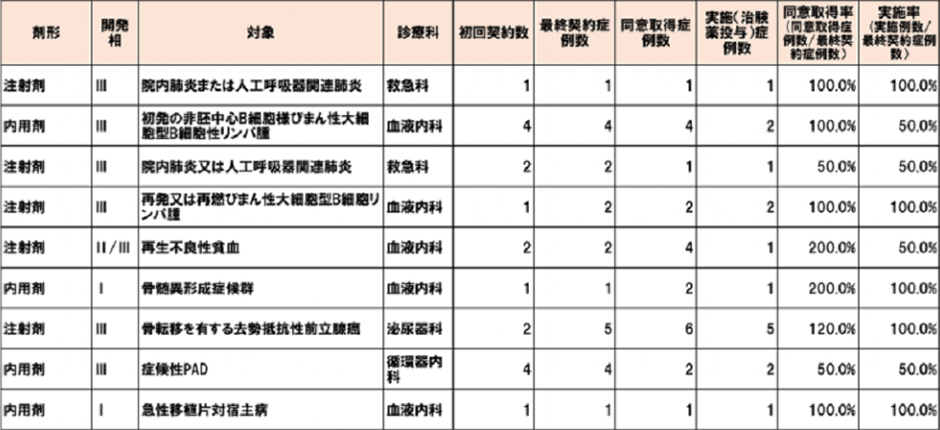
2018年度終了課題
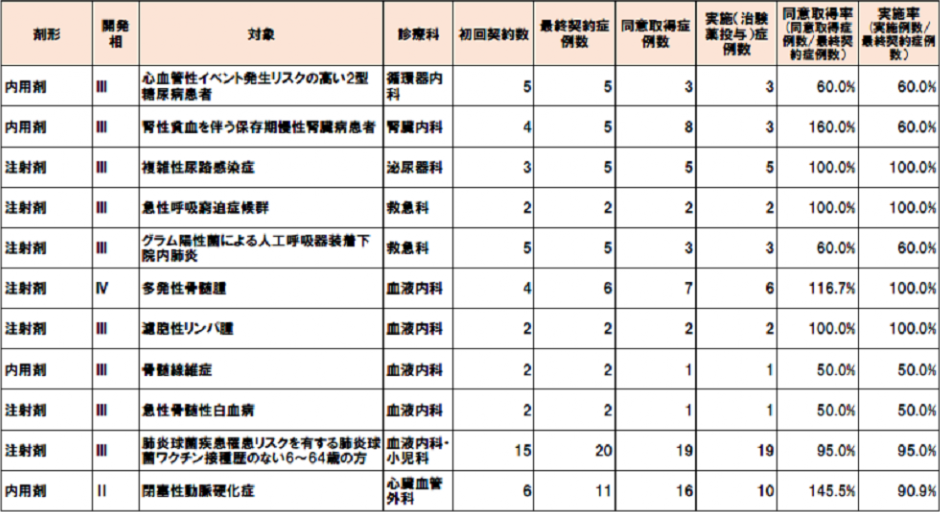
2017年度終了課題
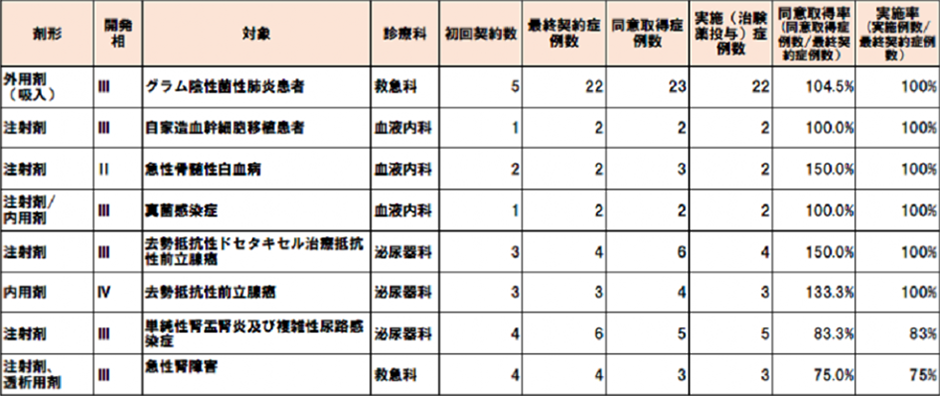
国際共同治験への取り組み
当院では2006年7月に最初の国際共同治験(試験)を受託し、2023年度3月31日現在、下表のとおり国際共同治験(試験)を受託しております。
| 2023 | 2022 | 2021 | 2020 | 2019 | 2018 | 2017 | 2016 | 2015 | 2014 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 救急科 | 1 | 1 | 1 | 1 | 3 | |||||
| 呼吸器内科 | 1 | |||||||||
| 循環器内科 | 2 | 1 | 1 | 1 | 2 | |||||
| 整形外科 | 1 | 1 | 1 | 2 | ||||||
| 血液内科 | 2 | 2 | 2 | 4 | 5 | 6 | 2 | 3 | 6 | 2 |
| 糖尿病・内分泌内科 | ||||||||||
| 脳神経内科 | 1 | |||||||||
| 泌尿器科 | 2 | 5 | 2 | 3 | 4 | 1 | 1 | 1 | ||
| 産婦人科 | 1 | |||||||||
| 腎臓内科 | 1 | |||||||||
| 外科 | 1 | 1 |
国立病院機構本部 中央治験審査委員会(NHO-CRB)について
国立病院機構熊本医療センター 中央治験審査委員会(KMC-CRB)の設置について
医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令(平成20年厚生労働省令第24号、平成20年2月29日の公布に伴い、平成21年2月12日に国立病院機構熊本医療センターに中央治験審査委員会「熊本医療センター 中央治験審査委員会(National Hospital Organization Kumamoto Medical Center Central Review Board)(略称KMC-CRB)」(以下、「KMC-CRB」という。)を設置・運営することといたしました。
なお、中央治験審査委員会は原則として毎月1回、第2水曜日(偶数月は15:00より、奇数月は15:30より開催)に開催いたします。
なお、中央治験審査委員会は原則として毎月1回、第2水曜日(偶数月は15:00より、奇数月は15:30より開催)に開催いたします。
